元素性质呈现周期性变化的基本原因是
| A.元素的原子量逐渐增大 | B.核外电子排布呈周期性变化 |
| C.核电荷数逐渐增大 | D.元素化合价呈周期性变化 |
下列各组离子在相应的条件下可以大量共存的是
| A.在碱性溶液中:CO32—、K+、C1—、Na+ |
| B.与铝粉反应放出氢气的无色溶液中:NO3—、Mg2+、Na+、SO42— |
| C.在c(H+)/c(OH—)==1×10—12的溶液中:NH4+、Ca2+、C1—、K+ |
| D.在中性溶液中:Fe3+、Na+、SCN—、C1— |
下列是某学生自己总结的一些规律,其中正确的是
| A.氧化物不可能是还原产物,只可能是氧化产物 |
| B.有些化学反应不属于化合、分解、置换、复分解中的任何一种反应 |
| C.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
| D.饱和溶液一定比不饱和溶液的浓度大 |
节能减排关系人类的生存环境,请从我做起。下列措施不属于“节能减排”的是
| A.及时关灯、关空调、关水龙头,节水、节电 |
| B.使用天然气热水器取代电热水器 |
| C.自2008年6月1日起,实行塑料购物袋有偿使用 |
| D.研制开发燃料电池汽车,减少机动车尾气污染 |
下图装置可用于收集气体X并验证其某些化学性质,你认为正确的是()
| 选项 |
气体 |
试剂 |
现象 |
结论 |
| A |
SO2 |
酸性KMnO4 |
溶液褪色 |
SO2有漂白性 |
| B |
NH3 |
酚酞溶液 |
溶液变红 |
氨水呈碱性 |
| C |
X |
澄清石灰水 |
溶液变浑浊 |
气体不一定是CO2 |
| D |
Cl2 |
紫色石蕊试液 |
溶液先变红后褪色 |
Cl2有酸性和漂白性 |
下图是反应 CO(g)+2H2(g)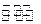 CH3OH(g)进行过程中的能量变化曲线。曲线 a表示不使用催化剂时反应的能量变化,曲线 b表示使用催化剂后的能量变化。下列相关说法正确的是()
CH3OH(g)进行过程中的能量变化曲线。曲线 a表示不使用催化剂时反应的能量变化,曲线 b表示使用催化剂后的能量变化。下列相关说法正确的是()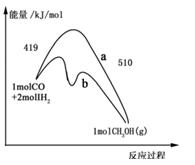
| A.其它条件不变,按曲线 b线进行的反应, CH3OH的产率更高 |
|
| B.其它条件不变,分别按曲线 a.b线进行的反应的热效应相同 | |
C.(1molCO + 2molH2)中的键能之和比 1molCH3OH中的键能之和大  |
D.热化学方程式为 CO(g)+2H2(g) CH3OH(g) △H=-91kJ·mol-1 |