X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
| A.元素Y、Z、W离子具有相同的电子层结构,其半径依次增大 |
| B.元素X与元素Y可以形成两种共价化合物,且这两种化合物只有一种类型的共价键 |
| C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
| D.元素W、R的最高价氧化物对应水化物都是强酸 |
氢氧化钡(固体)、硫酸铜(固体)、硫酸(纯液体)这些物质可以归为一类,下列哪种物质还可以和它们归为一类
| A.C2H5OH(液态) | B.豆浆 | C.水煤气 | D.HCl(气态) |
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如下图所示的转化关系(部分生成物和反应条件略去)。
下列推断不正确的是
A.若X是Na2CO3,C为仅含极性键的气体物质, 则A一定是氯气
B.若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E在一定条件下能还原CuO
C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
在250C、101kPa,1g甲醇燃烧生成二氧化碳和液态水放热22.7 kJ, 甲醇燃烧热的热化学方程式书写正确的是
A.CH3OH(l) + 3/2O2(g)= CO2(g) + 2H2O(l) △H= -726.4 kJ/mol
B.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H=" -1452.8" kJ/mol
C.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H= -726.4 kJ/mol
D.2CH3OH(l) + 3O2(g)= 2CO2(g) + 4H2O(l) △H= +1452.8 kJ/mol
X、Y是短周期元素,两者能形成化合物X2Y3,已知X的核电荷数为n,则Y的核电荷数不可能是
| A.n+11 | B.n+1 | C.n+3 | D.n+4 |
由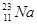 、
、 、
、 三种微粒构成的11.7g的氯化钠,其中
三种微粒构成的11.7g的氯化钠,其中 的质量是(氯的平均近似相对原子量为35.5)
的质量是(氯的平均近似相对原子量为35.5)
| A.1.85g | B.8.70g | C.7.11g | D.4.63g |