16O中的16表示的含义是( )
| A.氧元素的相对原子质量 |
| B.氧元素的一种同位素的近似相对原子质量 |
| C.氧元素的近似相对原子质量 |
| D.氧元素的一种同位素的质量数 |
mA(s)+nB(g)  pC(g);ΔH<0,在室温条件下B的体积分数(B%)与压强(P)的关系如图所示。
pC(g);ΔH<0,在室温条件下B的体积分数(B%)与压强(P)的关系如图所示。
则下列有关叙述中一定正确的是( )
①m+n<p ②X点时的正反应速率大于逆反应速率
③X点比Y点时的反应速率慢④若升高温度,该反应的平衡常数增大
| A.①②③ | B.②③④ | C.只有②③ | D.①②④ |
把80mlNaOH溶液加入到120ml盐酸中,所得溶液的PH值为2(设混合后溶液总体积为原溶液体积之和)。如果混合前NaOH溶液和盐酸的物质的量浓度相同,它们的浓度是()
| A.0.05mol/L | B.0.1mol/L | C.1.0mol/L | D.0.5mol/L |
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g),甲醇生成量与时间的关系如下图所示。
CH3OH(g),甲醇生成量与时间的关系如下图所示。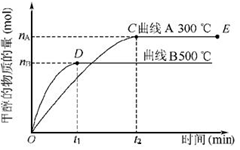
下列有关说法正确的是( )
| A.在300 ℃条件下,t1时刻该反应达到化学平衡 |
| B.在500 ℃条件下,从反应开始到平衡,氢气的平均反应速率v(H2)为nB/(3t1) mol/L |
| C.在其他条件不变的情况下,将处于E点的体系体积压缩到原来的1/2,则氢气的浓度减小 |
| D.由图像说明该反应的正反应为放热反应 |
一定温度下,在固定体积的密闭容器中发生可逆反应 A(s)+2B(g) 2C(g) ,下列叙述中是反应达到平衡的标志的是( )
2C(g) ,下列叙述中是反应达到平衡的标志的是( )
(1)v正(A)=2v逆(C);(2)单位时间生成amol A,同时生成2amol B;(3)A、B、C的浓度不再变化;(4)混合气体的平均摩尔质量不再变化(5)混合气体的总压强不再变化;(6)A、B、C的分子数目比为1:3:2。
A.(1)(3)(4)B.(3)(4) C.(2)(3)(5) D.(3)(4)(5)(6)
某酸甲溶液的pH=2,某酸乙溶液的pH=3,下列说法正确的是( )
| A.若甲为强酸、乙为弱酸,则c(甲) :c(乙)="10" :1 |
| B.若甲为弱酸,乙为强酸,则一定满足c(甲)>c(乙) |
| C.若甲为强酸,乙为弱酸,则其物质的量浓度不可能相等 |
| D.若甲、乙均为弱酸,则甲酸的电离常数一定比乙酸大 |