CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如下图所示,下列结论不正确的是 ( )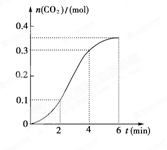
| A.反应开始2 min内平均反应速率最大 |
| B.反应速率先增大后又减小 |
| C.反应开始4 min内温度对反应速率的影响比浓度大 |
| D.反应在第2 min到第4 min间生成CO2的平均反应速率为 v (CO2)="0.1" mol·min-1 |
所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,根据下列四种金属的熔沸点,其中不能形成合金的是()
| Na |
Cu |
Al |
Fe |
|
| 熔点(0C) |
97.5 |
1083 |
660 |
1535 |
| 沸点(0C) |
883 |
2595 |
2200 |
3000 |
A.Cu和Al B.Fe和Cu C.Fe和Na D.Al和Na
下列每组分子主要能形成分子间氢键的是()
| A.HClO4 和 H2SO4 | B.CH3COOH和H2Se |
| C.C2H5OH和NaOH | D.H2O2和HNO3 |
下列分子中所有原子都满足最外层8电子结构的是()
①CO2 ②XeF6 ③PCl3 ④SO2 ⑤BF3 ⑥N2 ⑦P4 ⑧PCl5
| A.①③⑥⑦ | B.①④⑤ | C.①④⑥ | D.②③④⑤ |
已知33As、35Br位于同一周期。下列关系正确的是( )
| A.原子半径:As>Cl>P | B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- | D.酸性:H3AsO4> H2SO4>H3PO4 |
现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是 ()
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③>②>① | D.最高正化合价:③>②>① |