CO2、NO2、SO2是中学常见的氧化物,下列有关三种氧化物的叙述正确的是( )
| A.它们均可与水反应生成酸,所以都是酸性氧化物 |
| B.它们都是无色、密度比空气大的有毒气体 |
| C.人类活动中过度排放CO2、SO2和NO2,都会引起酸雨 |
| D.它们在反应中都可做氧化剂 |
.某物质的分子式为CxHyOz,取该物质a g在足量的O2中充分燃烧后,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了b g,且a > b,则该物质的分子式可能是
| A.C3H6O2 | B.C3H6O3 | C.CH2O2 | D.C3H8O3 |
盆烯、月桂烯、柠檬烯等萜类化合物广泛存在于动、植物体内,关于这些有机物的下列说法中正确的是
①盆烯、月桂烯、柠檬烯都能使溴水褪色②盆烯与苯互为同分异构体
③月桂烯、柠檬烯互为同分异构体④盆烯与氢气加成后的产物的一氯代物有四种
| A.①②④ | B.①②③④ | C.①②③ | D.①③ |
下列各组指定物质的同分异构体数目相等的是
| A.乙烷的二氯代物和丙烷的一氯代物 | B.丙烷的一氯代物和戊烷 |
| C.苯的二氯代物和苯的一硝基代物 | D.C3H6和C5H12 |
某烃的化学式为C4Hm,下列关于C4Hm的说法中正确的是
| A.当m=8时,该烃一定与乙烯互为同系物 |
| B.当m=4时,该烃一定含有碳碳双键 |
| C.该烃不可能同时含有碳碳双键和碳碳三键 |
| D.1mol C4Hm完全燃烧,不可能生成3.5mol H2O |
下列反应中,属于取代反应的是
①CH3CH=CH2+Br2 CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH=CH2+Br2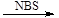 CH2BrCH=CH2+HBr
CH2BrCH=CH2+HBr
③ +HNO3
+HNO3
 +H2O
+H2O
④CH3CH2OH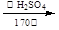 CH2=CH2↑+ H2O
CH2=CH2↑+ H2O
| A.②④ | B.③④ | C.①③ | D.②③\ |