25℃时,有c(CH3COOH)+c(CH3COO-)=" 0." 1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是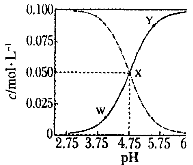
| A.X点所表示的溶液中:c(Na+)+ c(OH-) = c(CH3COO-) + c(H+) |
| B.W 点所表示的溶液中:c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=" 0." 1mol·L-1 |
| C.该温度下醋酸的电离平衡常数为10-4.75 mol·L-1 |
| D.向X点所表示的溶液中加入等体积的0. 05mol·L-1NaOH溶液:c(H+)= c(CH3COOH)+c(OH-) |
下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是
| A.盐酸、水煤气、醋酸、干冰 | B.天然气、空气、苛性钾、石灰石 |
| C.液氨、氯水、硫酸钠、乙醇 | D.胆矾、漂白粉、氯化钾、氯气 |
下列溶液中Cl-浓度与50 mL 1 mol·L-1 AlCl3溶液中Cl-浓度相等的是
| A.150 mL 1 mol·L-1的NaCl溶液 | B.75 mL 2 mol·L-1 NH4Cl溶液 |
| C.150 mL 2 mol·L-1的KCl溶液 | D.75 mL 1 mol·L-1的FeCl3溶液 |
有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)/mol·L-1为
| A.(y-2x)/a | B.(y-x)/a | C.(2y-2x)/a | D.(2y-4x)/a |
物质的量浓度相同的硝酸钾、硫酸钾、磷酸钾(K3PO4)三种溶液中,若使钾离子的物质的量相同,则这三种溶液的体积比为
| A.3:2:1 | B.6:3:2 | C.2:3:6 | D.1:2:3 |
X、Y、Z为三种单质。已知:Y能将Z从其化合物的水溶液中置换出来,而Z又能将X从其化合物中置换出来。由此可以推断下列说法中可能正确的是
①单质的氧化性:Y>Z>X;②单质的还原性:Y>Z>X;
③对应离子的氧化性:X>Z>Y;④对应离子的还原性:X>Z>Y
| A.只有① | B.只有②③ | C.只有①④ | D.①②③④ |