下列说法中,正确的是
| A.实验室可以用氢氧化钠溶液出去乙酸乙酯中的乙酸杂质 |
| B.乙烯和聚乙烯都可以和溴水发生加成反应 |
| C.汽油、柴油和植物油的主要成分都是碳氢化合物 |
| D.分子式同为C3H7Cl,但沸点不同的分子共有两种 |
下列各组液体混和物,用分液漏斗不能分离的是
| A.苯和水 | B.四氯化碳和水 | C.乙酸和水 | D.正己烷和水 |
有三个热化学方程式:① 2H2 (g) + O2 (g) = 2H2O (g) ,放出 Q1 kJ的热量;
② 2 H2 (g) + O2 (g) =" 2" H2O (l) ,放出Q2 kJ的热量;
③ H2 (g) + 1/2 O2 (g) = H2O (g) ,放出 Q3 kJ的热量;
则Q1、Q2、Q3的大小关系为
| A.Q1 = Q2 = Q3 | B.2Q3 = Q1 < Q2、 |
| C.Q3 < Q2 < Q1 | D.Q1 < Q2 < 3Q3 |
航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其化学方程式可表示为:
2NH4ClO4 = N2↑+ 4H2O↑+ Cl2↑+ 2O2↑(该反应为放热反应)下列对此反应的叙述中错误的是
| A.上述反应属于分解反应 |
| B.上述反应瞬间产生大量高温气体推动航天飞机飞行 |
| C.反应从能量变化上说,主要是化学能转变为热能和动能 |
| D.在反应中高氯酸铵只起氧化剂作用 |
在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s)+2B(g)  C(g)+D(g)已达到平衡状态
C(g)+D(g)已达到平衡状态
①混合气体的压强 ②混合气体的密度 ③各气体物质的物质的量浓度 ④气体的总物质的量⑤混合气体的平均相对分子质量
| A.②③⑤ | B.①②③ |
| C.②③④⑤ | D.①③④⑤ |
工业上用氮气和氢气合成氨:N2+3H2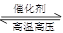 2NH3(反应放热),从反应速率和化学平衡两方面看,合成氨的适宜条件一般为压强:20 MPa—50 MPa,温度:500 ℃左右,催化剂:铁触媒。下列有关合成氨工业的叙述不正确的是
2NH3(反应放热),从反应速率和化学平衡两方面看,合成氨的适宜条件一般为压强:20 MPa—50 MPa,温度:500 ℃左右,催化剂:铁触媒。下列有关合成氨工业的叙述不正确的是
| A.使用铁触媒,可使氮气和氢气混合气体之间的反应在较低温度下取得较高的反应速率 |
| B.工业上选择上述条件下合成氨,可以使氮气全部转化为氨 |
| C.上述化学平衡的移动受到温度、反应物的浓度、压强等因素的影响 |
| D.温度升高,不利于氮气的转化率 |