将1 mol CO和2 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g)=CH3OH(g),ΔH="a" kJ/mol,如图。下列分析中正确的是
A.250°C时,0〜10minH2反应速率为 0.015 mol,/(L.min)
B.平衡时CO的转化率:T℃时小于250℃时
C.其他条件不变,若减小容积体积,CO体积分数增大
D.a<0,平衡常数K:T0C时大于2500C
向Fe2(SO4)3、CuCl2混和溶液中投入足量的铁粉充分反应后,得到的固体经过滤、干燥、称重,若所得固体的质量与加入的铁粉的质量相等,则原溶液中c(SO42-)与c(Cl-)之比为:
| A.3︰14 | B.1︰7 | C.2︰7 | D.3︰2 |
正在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过H2O。以下叙述正确的是
| A.硫酸盐都易溶于水 |
| B.检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品―→粉碎―→加水溶解―→过滤―→向滤液中滴加KSCN溶液 |
| C.分别还原a mol Fe2O3所需H2、Al、CO物质的量之比为3∶2∶3 |
| D.明矾含有结晶水,是混合物 |
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是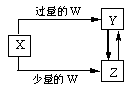
| 选项 |
W |
X |
| A |
盐酸 |
Na2CO3溶液 |
| B |
NaOH溶液 |
AlCl3溶液 |
| C |
CO2 |
Ca(OH)2溶液 |
| D |
Cl2 |
Fe |
某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是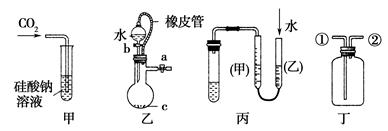
| A.甲装置:可用来证明碳酸的酸性比硅酸强 |
| B.乙装置:橡皮管的作用是能使水顺利流下 |
| C.丙装置:用图示的方法不能检查此装置的气密性 |
| D.丁装置:先从①口进气集满二氧化碳,再从②口进气,可收集氢气 |
某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:2A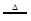 B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
B+2C+2D,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为
| A.2d | B.10d | C.5d | D.0.8d |