下列叙述正确的是
| A.硅是一种重要的非金属单质,可用于制造太阳能电池 |
| B.硫在足量的空气中燃烧生成SO3 |
| C.钠在空气中燃烧生成氧化钠 |
| D.与同浓度稀盐酸反应的速率:Na2CO3>NaHCO3 |
向盛有一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似的用下图中的曲线表示是()
设NA表示阿伏加德罗常数的值,下列表述 不正确的是()
不正确的是()
| A.标准状况下,22.4L氢气所含质子数是2NA |
| B.5.4g水所含的分子数为0.3NA |
| C.含1mol硫酸钾的溶液中硫酸根离子数为2NA |
| D.1mol金属钠与水反应失去的电子数为NA |
下列关于物质的量浓度表述正确的是()
| A.0.3 mol·L-1的Na2SO4溶液中含有Na+和SO的总物质的量为0.9 mol·L-1 |
| B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,只有当22.4 L(标况)氨气溶于水制得1 L氨水时,其浓度才是1 mol·L-1 |
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO的物质的量相等,则K+和Cl-的物 质的量浓度一定相同 质的量浓度一定相同 |
D.10 ℃时,100 ml 0.35 mol/L的KCl饱和溶液蒸发掉5 g水,冷却到10 ℃时,其体积小于100 ml,它的物质 的量浓度仍为0.35 mol/L 的量浓度仍为0.35 mol/L |
在下列反应中, HCl 作氧化剂的是()
| A.NaOH+HCl=NaCl+H2O |
| B.Zn+2HCl=ZnCl2+H2↑ |
C.MnO2+4HCl(浓) 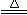 MnCl2+2H2O+Cl2↑ MnCl2+2H2O+Cl2↑ |
| D.CuO+2HCl=CuCl2+H2O |
11P+ 15CuSO4+ 24H2O = 5Cu3P+ 6H3PO4 + 15H2SO4反应中,被氧化的P原子与被还原的P原子个数比是 ()
| A.6:5 | B.5:6 | C.11:5 | D.11:6 |