下列说法正确的是
A.用氯酸钾固体和浓盐酸制氯气的反应方程式: |
| B.向含有大量Ca2+、Cl—、Al3+的溶液中通入适量SO2,有沉淀生成 |
| C.用少量酸性KMnO4溶液可以检测FeCl3浓溶液中是否含有Fe2+ |
| D.常温下Ksp[Cu(OH)2]=2.2×10-20,则常温下2.2mol/L CuCl2溶液的pH不大于4 |
利用下图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是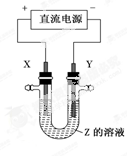
| A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 |
| B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 |
| C.电镀工业中,X是待镀金属,Y是镀层金属 |
| D.外加电流的阴极保护法中,Y是待保护金属 |
2008年,美籍华裔科学家钱永健获得2008年度诺贝尔化学奖。16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获“美国西屋天才奖”。下列叙述正确的是
| A.金属腐蚀就是金属失去电子被还原的过程 |
| B.水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
| C.纯银质物品久置表面变暗,是银发生吸氧腐蚀的结果 |
| D.钢板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e-==Fe3+,继而形成铁锈 |
把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是
| A.10℃20mL 3mol/L的X溶液 | B.20℃30mL 2mol/L的X溶液 |
| C.20℃10mL 4mol/L的X溶液 | D.10℃10mL 2mol/L的X溶液 |
下列装置中,都伴随有能量变化,其中是由化学能转变为电能的是



| A.电解水 | B.水力发电 | C.太阳能热水器 | D.干电池 |
下列说法不正确的是
| A.开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B.废旧电池不能随意丢弃,要进行深埋处理,防止重金属污染 |
| C.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 |
| D.使用分光光度计,可以换算得到某溶液的浓度 |