二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色的气体,易溶于水。实验室可用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料来制备ClO2,其流程如下:
(1)写出电解时发生反应的化学方程式: 。
(2)除去ClO2中的NH3可选用的试剂是 。(填字母)
| A.饱和食盐水 | B.碱石灰 | C.浓硫酸 | D.水 |
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收;将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去VmL硫代硫酸钠溶液。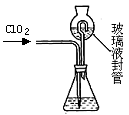
①装置中玻璃液封管的作用是 ; 。
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式 。
③滴定终点的现象是: 。
④测得通入ClO2的质量m(ClO2)= 。(用含c、V的代数式表示)(已知:ClO2的相对分子质量为67.5)
(4)设计实验来确定溶液X的成分,请补充完成实验步骤和现象。
| 实验步骤 |
实验现象 |
实验结论 |
| ① |
|
溶液X中含有Na+ |
| ② |
|
溶液X中含有Cl- |
某工业废水中仅含下表离子中的5种,且各种离子的物质的量浓度相等,均为0.1mol/L。
| 阳离子 |
K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 |
Cl-CO32- NO3- SO42- SiO32- |
欲探究废水的组成,进行如下实验:Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ. 向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)仅由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是(写离子符号)。
(2)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为:
_______________________________________________________________
(3)原溶液中所含阳离子是,阴离子是。(写离子符号)
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。
Ⅰ:在试管中加入3 mL 1 mol/L NaOH溶液和3 mL 溴乙烷,振荡,加热。
(1)设计实验证明上述实验中溴乙烷里的Br变成了Br-
(需说明:简单的实验操作及预测产生的实验现象)。
(2)观察到现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是和。
II:在试管中加入3 mL NaOH乙醇溶液和3 mL 溴乙烷,振荡,加热。
设计实验证明上述实验中溴乙烷发生的是消去反应
(需说明:简单的实验操作及预测产生的实验现象)。
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+ O2 (g)  2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
2SO3(g) △H< 0。查阅资料知SO3熔点16.83℃,沸点44.8℃。
(1)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2,O2,SO3物质的量变化如图。
①该反应的化学平衡常数表达式 K=
②该反应能自发进行的原因是。
③据图判断,该反应处于平衡状态的时间是。
④据图判断,反应进行至20 min时,曲线发生变化的原因是(用文字表达)。
(2)某化学研究学习小组用下图的装置组装设计了一个实验,以测定SO2转化为SO3的转化率,仪器的连接顺序是a→h→i→b→c→f→g→d→e。
①为提高SO2的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是。
②在Ⅰ处用大火加热烧瓶时SO2的转化率会。(填“填大”“不变”或“减小”)
③用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重 m g,则本实验中SO2的转化率为。
用一定物质的量浓度的NaOH溶液滴定10.00 mL已知浓度的盐酸,滴定结果如图所示。回答下列问题:
(1)有关滴定的操作可分解为如下几步,并补充完整。①用NaOH溶液润洗滴定管。②取NaOH溶液注入碱式滴定管至“0”刻度以上2~3 mL。③④调节液面至“0”或“0”刻度以下,记下读数。⑤移取10.00 mL盐酸注入锥形瓶中,加入酚酞。⑥把锥形瓶放在滴定管的下面,用氢氧化钠溶液滴定并记下读数。
(2)若滴定前俯视滴定管读数,滴定后平视刻度读数,则会使氢氧化钠浓度的测定结果(填“偏高”“偏低”或“不变”)。
(3)如用酚酞作指示剂,则滴定终点的实验现象是。
(4)c(HCl)=mol·L-1
(5)c(NaOH) =mol·L-1
(6)右图表示50 mL滴定管中液面的位置,如果液面处的读数是a ,则滴定管中液体的体积(填代号)。
| A.是a mL | B.是(50-a)mL |
| C.一定大于a mL | D.一定大于(50-a)mL |
(7)常温下,用0.01 mol•L-1H2SO4溶液滴定0.01 mol•L-1 NaOH溶液,中和后加水至100 ml。若滴定到终点时少加一滴H2SO4(设1滴为0.05 ml)。则此时溶液的pH为。
某同学用如图一所示装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有看到浑浊现象。经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓缓地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象。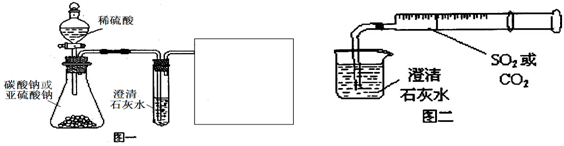
(1)SO2是空气污染物之一,它的危害是。
(2)图一中生成CO2反应的离子方程式为;
(3)如何鉴别CO2和SO2(只需要写出一种方法,应写出操作方法、现象和结论)?。
(4)用图一进行SO2与石灰水反应的实验时,从环保角度考虑,还需要增加什么装置,在方框中画出。
(5)对比分析两组实验,你认为用图一装置实验时,通过SO2不能出现浑浊的原因可能是。