氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。利用FeO/Fe3O4循环制氢,已知:
H2O(g)+3FeO(s) Fe3O4(s)+4H2(g) △H=akJ/mol (I)
Fe3O4(s)+4H2(g) △H=akJ/mol (I)
2Fe3O4(s) 6FeO(s)+O2(g) △H=bkJ/mol (II)
6FeO(s)+O2(g) △H=bkJ/mol (II)
下列坐标图分别表示FeO的转化率(图-1 )和一定温度时,H2出生成速率[细颗粒(直径0.25 mm),粗颗粒(直径3 mm)](图-2)。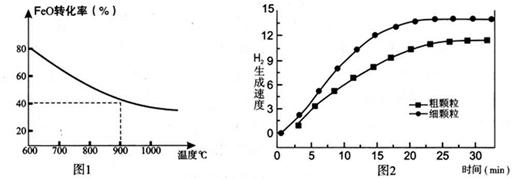
(1)反应:2H2O(g)=2H2(g)+O2(g) △H= (用含a、b代数式表示);
(2)上述反应b>0,要使该制氢方案有实际意义,从能源利用及成本的角度考虑,实现反应II可采用的方案是: ;
(3)900°C时,在两个体积均为2.0L密闭容器中分别投人0.60molFeO和0.20mol H2O(g)甲容器用细颗粒FeO、乙容器用粗颗粒FeO。
①用细颗粒FeO和粗颗粒FeO时,H2生成速率不同的原因是: ;
②细颗粒FeO时H2O(g)的转化率比用粗颗粒FeO时H2O(g)的转化率 (填“大”或“小”或“相等”);
③求此温度下该反应的平衡常数K(写出计箅过程,保留两位有效数字)。
(4)在下列坐标图3中画出在1000°C、用细颗粒FeO时,H2O(g)转化率随时间变化示意图(进行相应的标注)。
常温下有pH=12的NaOH溶液100mL,要使它的pH为11(体积变化忽略不计)
(1)如果加入蒸馏水,应加_________mL;
(2)如果加0.01mol/L HCl,应加_________mL
实验室里常利用反应:3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O来制取NO,当有6.4gCu参加反应时,计算:
3Cu(NO3)2+2NO↑+4H2O来制取NO,当有6.4gCu参加反应时,计算:
(1)能生成多少升NO(标准状况下)?
(2)消耗多少摩HNO3?
(3)被还原的HNO3的物质的量?
有三种饱和一元醇(通式为CnH2n+2O)A、B、C,其相对分子质量比为8︰15︰22。按其物质的量的比为1︰2︰1混合,取该混合液12g与足量钠反应,生成标准状况下的氢气的体积为2.24L。求A、B、C的分子式。
某液化石油气由丙烷和丁烷组成,其质量分数分别为80%和20%,它们燃烧的热化学方程式分别为
C3H8(g)+5O2(g)→3CO2(g)+4H2O(g) △H=–2200KJ·mol-1
2C4H10(g)+13O2(g)→8CO2(g) +10H2O(g)△H=–5800KJ·mol-1
有一质量为0.8Kg、容积为4.0L的铝壶,将一壶20℃的水烧开需消耗该液化石油气0.056Kg。试计算该燃料的利用率[已知水的比热为4.2KJ/(Kg·℃),铝的比热为0.88KJ/(Kg·℃)]
丙酮和碘在酸性溶液中发生下列反应:CH3COCH3+I2 → CH3COCH2I +H+ +I-。 25℃ 时,该反应的速率由下列经验式决定:v=2.73×10-5c(CH3COCH3)c(H+) mol/(L•s)。
25℃时,如果c(I2)、c(CH3COCH3)、c(H+)的起始浓度依次是0.01mol/L、0.1mol/L、0.01mol/L,求:
(1)反应开始时的速率是多少?
(2)当溶液中的I2消耗一半时,反应速率比开始时慢还是快