在固定体积的密闭容器中进行如下反应:2SO2(g) + O2(g)  2 SO3(g)。已知反应过程某一时刻SO2、O2、SO3浓度(mol•L-1)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( )
2 SO3(g)。已知反应过程某一时刻SO2、O2、SO3浓度(mol•L-1)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( )
| A.SO2、O2分别为0.4mol•L-1、0.2mol•L-1 | B.SO2为0.25mol•L-1 |
| C.SO2、SO3均为0.15mol•L-1 | D.SO3为0.4mol•L-1 |
下列叙述中正确的是
| A.进行H2O和H2S的热分解实验,可确定S、O两种元素的非金属性强弱 |
| B.根据非金属性强弱F>Cl,可以推测沸点HF>HCl |
C.已知2C+SiO2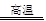 Si+2CO↑,说明C的非金属性比Si强 Si+2CO↑,说明C的非金属性比Si强 |
| D.H2SO3的酸性比H2CO3的酸性强,说明S的非金属性比C强 |
可逆反应2NO2 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n molNO
②单位时间内生成n mol O2的同时生成2n molNO2
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
| A.①④ | B.②④ | C.①③④ | D.①②③④⑤ |
一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g) H2(g)+I2(g)。若c(HI)由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么c (HI)由0.07 mol·L-1降到0.05 mol·L-1时,所需反应的时间为
H2(g)+I2(g)。若c(HI)由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么c (HI)由0.07 mol·L-1降到0.05 mol·L-1时,所需反应的时间为
| A.等于5 s | B.等于10 s |
| C.大于10 s | D.小于10 s |
某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气。所用燃料为氢气,电解质为熔融的碳酸钾。已知电极反应如下:总反应:2H2+O2===2H2O,正极反应:O2+2CO2+4e-===2CO32— 下列推断正确的是
| A.负极反应为H2+2OH--2e-===2H2O |
| B.该电池可在常温或高温时进行工作,对环境具有较强的适应性 |
| C.该电池供应2 mol水蒸气,同时转移2 mol电子 |
| D.放电时负极有CO2生成 |
镁/H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是
| A.电池总反应为Mg+H2O2===Mg(OH)2 |
| B.正极发生的电极反应为H2O2+2H++2e-===2H2O |
| C.工作时,正极周围海水的pH减小 |
| D.电池工作时,溶液中的H+向负极移动 |