下列反应的离子方程式正确的是
| A.向稀氨水中加入稀盐酸 OH- + H+ =H2O |
| B.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| C.碳酸钙溶于醋酸中 CaCO3 + 2H+ =Ca2+ + H2O + CO2↑ |
| D.碳酸氢钙溶液跟稀硝酸反应 HCO3-+ H+ = H2O + CO2↑ |
某有机物ng,跟足量金属钠反应生成vLH2,另取ng该有机物与足量碳酸氢钠作用生成vLCO2(同一状况),该有机物分子中含有的官能团为
| A.含一个羧基和一个羟基 | B.含两个羧基 |
| C.只含一个羧基 | D.含两个羟基 |
白藜芦醇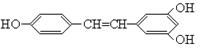 广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是
广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是
| A.1mol 1 mol | B.3.5 mol 7 mol |
| C.3.5 mol 6 mol | D.6 mol 7 mol |
胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法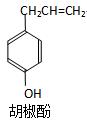
①该化合物属于芳 香烃
香烃
②分子中至少有7个碳原子处于同一平面
③它的部分同分异构体能发生银镜反应
④1mol该化合物最多可与2molBr2发生反应。其中正确的是
A.①③  |
B.①②④ | C.②③ | D.②③④ |
下列文字表述与反应方程式对应且正确的是
| A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓ |
| B.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑ |
| C.利用腐蚀法制作印刷线路板:Fe3+ + Cu ="=" Fe2+ + Cu2+ |
D.实验室用液溴和苯在催化剂作用下制溴苯: |
利尿酸在奥运会上被禁用,其结构简式如图所示.下列叙述正确的是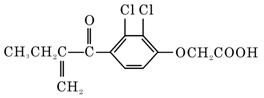
| A.利尿酸衍生物利尿酸甲脂的分子式是C14H14Cl2O4 |
| B.利尿酸分子内处于同一平面的原子不超过10个 |
C.1 mol利尿酸能与7 mol H2发生加成反应 H2发生加成反应 |
| D.利尿酸能与FeCl3溶液发生显色反应 |