反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示,下列说法正确的是
C(g) +D(g)过程中的能量变化如图所示,下列说法正确的是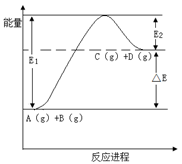
| A.该反应是放热反应 |
| B.加入催化剂后,反应加快,△E减小 |
| C.反应物的总键能大于生成物的总键能 |
| D.反应达到平衡时,升高温度,A的转化率增大 |
下列食品添加剂与其说明错误的是
| A.食醋——酸味剂 | B.亚硝酸钠——咸味剂 |
| C.碳酸氢钠——疏松剂 | D.苯甲酸——防腐剂 |
下表是小王同学血常规检查报告单中的部分内容
| 编号 |
项目 |
结果 |
正常范围参考值 |
单位 |
| 1 |
红细胞计数 |
2.3 |
3.5~5 |
×1012·L-1 |
| 2 |
血红蛋白 |
75 |
110~150 |
g·L-1 |
小王同学应注意补充的微量元素是
A.硒 B.锌 C.铁 D.碘
下列关于维生素C的说法中,不正确的是
| A.能防治坏血病,又称为抗坏血酸 | B.属于水溶性维生素 |
| C.有强氧化性 | D.主要存在于水果和新鲜蔬菜中 |
如果人体摄入的油脂中饱和酯太多,就容易发胖,可能引发高血压、高血脂等疾病。下列油脂中饱和酯含量最高的是
| A.豆油 | B.花生油 | C.芝麻油 | D.牛油 |
下列关于药物的使用说法正确的是
| A.虽然药物能治病,但大部份药物有毒副作用 |
| B.青霉素有解热镇痛的作用 |
| C.阿司匹林是最重要的抗生素 |
| D.随着药物的普及,生病了都可以到药店自己买药吃,不用到医院 |