以下是一些物质的熔沸点数据(常压):
| |
钾 |
钠 |
Na2CO3 |
金刚石 |
石墨 |
| 熔点(℃) |
63.65 |
97.8 |
851 |
3550 |
3850 |
| 沸点(℃) |
774 |
882.9 |
1850(分解产生CO2) |
---- |
4250 |
金属钠和CO2在常压、890℃发生如下反应:
4 Na(g)+ 3CO2(g) 2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
2 Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
(1)上述反应的平衡常数表达式为 ;若4v正(Na)=3v逆(CO2),反应是否达到平衡 (选填“是”或“否”)。
(2)若反应在10L密闭容器、常压下进行,温度由890℃升高到1680℃,若反应时间为10min, 金属钠的物质的量减少了0.20mol,则10min里CO2的平均反应速率为 。
(3)高压下有利于金刚石的制备,理由是 。
(4)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
(5)下图开关K接M时,石墨作 极,电极反应式为 。K接N一段时间后测得有0.3mol电子转移,作出y随x变化的图象〖x—代表n(H2O)消耗,y—代表n[Al(OH)3],反应物足量,标明有关数据〗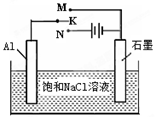

标准状况下,H2和CO的混合气体共8.96L,测得其质量为6.0g,试计算此混合气体中H2和CO的质量和体积各为多少?
10g碳酸钙与足量盐酸反应,消耗盐酸的物质的量为多少?生成二氧化碳气体的体积(标准状况)为多少?
在标准状况下,2.24L HCl气体的质量为多少,将其溶于水,配成500ml盐酸溶液,所得溶液的H+ 的物质的量浓度?
常温下,在32.0g水中溶解8.0g CuSO4粉末,恰好达到饱和,该溶液密度为1.2g/cm3,求:(1)该溶液中CuSO4的物质的量浓度。
(2)取出20.0ml该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
将26克含有SiO2和CaCO3固体在高温下加热至质量不再改变,冷却后称重为17.2克。(已知:SiO2 + CaCO3CaSiO3 + CO2↑,SiO2和CaSiO3均为固体)
(1)求生成的CO2的体积(标准状况下)
(2)求原混合物中所含SiO2的质量。