碘钨灯比白炽灯使用寿命长。灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g) WI2(g) ΔH<0(温度T1<T2)。下列说法正确的是
WI2(g) ΔH<0(温度T1<T2)。下列说法正确的是
| A.灯管工作时,扩散到灯丝附近高温区的WI2(g)会分解出W,W重新沉积到灯丝上 |
| B.灯丝附近温度越高,WI2(g)的转化率越低 |
C.该反应的平衡常数表达式是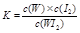 |
| D.利用该反应原理可以提纯钨 |
有以下两个反应:C+CO2 2CO;(正反应为吸热反应;反应速率为v1),
2CO;(正反应为吸热反应;反应速率为v1),
N2+3H2 2NH3;(正反应为放热反应;反应速率为v2),当温度升高时,v1和 v2的变化情况为( )
2NH3;(正反应为放热反应;反应速率为v2),当温度升高时,v1和 v2的变化情况为( )
| A.同时增大 | B.同时减小 | C.增大,减小 | D.减小,增大 |
下列说法正确的是( )
| A.1mol可燃物燃烧生成氧化物放出的热量就是该物质的燃烧热 |
| B.因为醋酸是弱电解质,盐酸是强电解质,所以中和等体积等物质的量浓度的醋酸和盐酸时,中和醋酸消耗的NaOH比盐酸消耗的NaOH用量少 |
| C.反应物总能量大于生成物总能量的反应是放热反应 |
| D.强电解质溶液的导电能力比弱电解质溶液的导电能力强 |
某一反应在一定条件下的平衡转化率为25.3%,其他条件不变,有一催化剂存在时,其转化率为()
| A.大于25.3% | B.小于25.3% | C.等于25.3% | D.约等于25.3% |
下列电离方程式的书写正确的是()
A. 2H2O  H3O++OH- H3O++OH- |
B. NaHCO3====Na++H++ |
C. NaHSO4 Na++H++ Na++H++ |
D. H2S  2H+ + S2- 2H+ + S2- |
下列说法正确的是 ()
| A.活化分子相互碰撞即可发生化学反应 |
| B.升高温度会加快化学反应速率,其原因是增加了活化分子的百分率 |
| C.某一反应的活化分子百分率是个定值 |
| D.浓度增大使得反应物分子中的活化分子百分率增大 |