下列实验能达到目的的是
| A.用CCl4萃取碘水中的碘 |
| B.将足量盐酸加入混有少量CaCO3杂质的Na2SO4中可除去杂质 |
| C.将混有少量HCl的Cl2通入NaOH溶液中除去HCl |
| D.将Fe(OH)3固体加入沸水中制备Fe(OH)3胶体 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是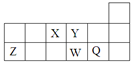
| A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)>r(Z3+) |
| B.元素W的最高价氧化物对应水化物的酸性比Q的强 |
| C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
| D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |
二甲醚是一种绿色、可再生的新能源。如图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极)。该电池工作时,下列说法不正确的是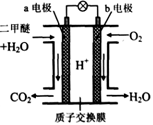
| A.a电极为该电池负极 |
| B.O2在b电极上得电子,被氧化 |
| C.电池工作时,a电极反应式: CH3OCH3—12e-+3H2O→2CO2↑+12H+ |
| D.电池工作时,燃料电池内部H+从a电极移向b电极 |
下列表示对应化学反应的离子方程式正确的是
| A.工业电解饱和食盐水:2Cl-+H2O=Cl2↑+H2↑+OH- |
B.碳酸钠的水解:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
| C.硫酸铝溶液中滴加过量浓氨水:Al3++4OH-=AlO2-+2H2O |
| D.用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,0.05 mol·L-1Fe2(SO4)3溶液中含Fe3+数目为0.1 NA |
| B.标准状况下,22.4L甲苯中含C—H数目为8 NA |
| C.常温、常压下,1.6g O2和O3混合物中,氧原子的数目为0.1NA |
| D.0.1mol Na2O2与足量CO2反应时,转移的电子数目为0.2 NA |
下列物质的转化在给定条件下能实现的是
①NaAlO2(aq) AlCl3
AlCl3 Al② NH3
Al② NH3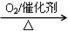 NO
NO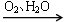 HNO3
HNO3
③NaCl(饱和) NaHCO3
NaHCO3 Na2CO3④FeS2
Na2CO3④FeS2 SO3
SO3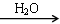 H2SO4
H2SO4
| A.②③ | B.①④ | C.②④ | D.③④ |