钛白粉(主要成分是TiO2),广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂。下图是以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料生产钛白粉并获得副产品FeSO4·7H2O的工艺流程图。
(1)钛铁矿与硫酸发生反应①的化学方程式为 ;在TiOSO4和FeSO4溶液中加入Fe的目的是 。
(2)溶液Ⅱ中TiOSO4在加热条件下发生水解反应②的离子方程式为 ;可回收利用的物质是 。
(3)为测定溶液Ⅱ中TiOSO4的含量,首先取待测钛液10 mL用水稀释至100 mL,加过量铝粉,充分振荡,使其完全反应:3TiO2+ +Al+6H+=3Ti3++Al3++3H2O。过滤后,取出滤液20.00 mL,向其中滴加2~3滴KSCN溶液作指示剂,用 (填一种玻璃仪器的名称)滴加0.1000mol·L-1 FeCl3溶液,当溶液出现红色达到滴定终点,用去了30.00mL FeC13溶液。待测钛液中TiOSO4的物质的量浓度是 。
在温度为373K时,把0.25moi NO2气体通入体积为500ml的真空密闭容器中,发生反应:2NO2(g)  N2O4(g) .反应进行到2s时,N2O4含量为0.05mol,进行到60s时,达到该条件下反应的最大限度,此时容器中混合气体的平均相对分子质量为47.5,则:
N2O4(g) .反应进行到2s时,N2O4含量为0.05mol,进行到60s时,达到该条件下反应的最大限度,此时容器中混合气体的平均相对分子质量为47.5,则:
(1)开始时2s内以c (NO2)的变化表示的反应速率是多少?
(2)达到最大限度时体系内的压强是开始的多少倍?
已知:2H2 ( g ) + O2 ( g ) = 2H2O ( l );△H = -571.6kJ/mol
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g );△H = -890 kJ/mol
标准状况下,取甲烷和氢气的混合气体11.2 L完全燃烧后恢复到常温,放出的热量为203.32kJ,试求混合气体中甲烷和氢气体积比.
在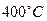 时,将
时,将 和
和 压入一个盛有催化剂的
压入一个盛有催化剂的 密闭容器中进行反应(
密闭容器中进行反应(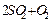

 ),2分钟时容器中剩下
),2分钟时容器中剩下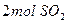 和
和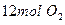 。则:
。则:
(1)2分钟内生成的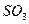 的物质的量是多少?
的物质的量是多少? 起始的物质的量是多少?
起始的物质的量是多少?
(2)2分钟内以 浓度变化表示的平均反应速率是多少?以
浓度变化表示的平均反应速率是多少?以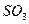 浓度变化表示的平均反应速率又是多少?
浓度变化表示的平均反应速率又是多少?
一定量的氢气在氯气中燃烧,所得混合物用100mL 4.00mol/L的NaOH溶液(密度为1.20g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0. 0800mol。(以下计算要有计算过程)
(1)求原NaOH溶液的质量分数为多少?
(2)求所得溶液中Cl-的物质的量。
(3)所用氯气和参加反应的氢气的物质的量之比为多少?
将一定量的SO和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
请回答下列问题:
(1)判断该反应达到平衡状态的标志是。(填字母)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是。(填字母)
a.向装置中再充入N2b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)求该反应达到平衡时SO3的转化率(用百分数表示)。
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?