下列离子方程式书写正确的是
| A.将铜屑加入Fe3+溶液中:Fe3++Cu=Fe2++Cu2+ |
B.NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| C.稀硝酸和过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
| D.KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+ =2H2O+I2 |
下列说法正确的是:()
| A.需要加热才能发生的反应一定是吸热反应 |
| B.在甲烷燃烧反应中,化学能只转化为热能 |
| C.旧化学键断裂吸收的能量与新化学键形成所释放的能量的相对大小决定了反应是放热还是吸热 |
| D.吸热反应在常温下不能发生 |
某元素原子序数为85,下面关于该元素说法不正确的是:()
| A.AgAt 不溶于水 |
| B.HAt很不稳定 |
| C.At的单质是白色固体 |
| D.该元素位于元素周期表第六周期、第十七列 |
关于原电池说法不正确的是:( ) 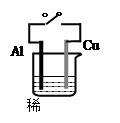
| A.右图所示原电池中,Cu为正极 |
| B.右图所示原电池中,开关闭合时,化学能主要转变为电能;断开时,化学能主要转变为热能 |
| C.在原电池中,负极上发生氧化反应,正极上发生还原反应 |
| D.在原电池中,电子从负极经过电解质溶液流向正极 |
下列各组物质的性质比较中,不正确的是:()
| A.金属性强弱:Na >Mg>Al | B.氢化物稳定性:HF > H2O >NH3 |
| C.碱性强弱:KOH>NaOH>LiOH | D.酸性强弱:HIO4 >HBrO4>HClO4 |
下列实验中,可以加快反应速率的是:( )
| A.钠与水反应时,增加水的量 |
| B.锌与稀硫酸反应时,加入少量CuSO4固体 |
| C.用18mol/L的硫酸溶液代替 2mol/L硫酸溶液常温下与铝反应 |
| D.合成氨反应,恒容通入氦气 |