燃料电池是利用燃料(如H2、CO、CH4等)跟氧气反应从而将化学能转化成电能的装置。下列关于甲烷燃料电池(NaOH溶液作电解质)的说法中正确的是
| A.负极反应为:O2+2H2O+ 4e-= 4OH- |
| B.负极反应为:CH4+ 10OH-- 8e-= CO32- + 7H2O |
| C.放电时正极发生氧化反应,外电路中电子从正极流向负极 |
| D.随着放电的进行,溶液的pH保持不变 |
下列离子方程式正确的是( )
| A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B.双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O |
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O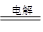 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| D.Na2S2O3溶液中加入稀硫酸:2S2O32—+4H+=SO32—+3S↓+2H2O |
下列解释事实的方程式不正确的是( )
| A.用浓盐酸检验氨:NH3+HCl=NH4Cl |
B.碳酸钠溶液显碱性:CO32—+H2O HCO3—+OH- HCO3—+OH- |
| C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ |
| D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O |
8.34 g FeSO4·7H2O样品在隔绝空气条件下受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。下列说法中正确的是()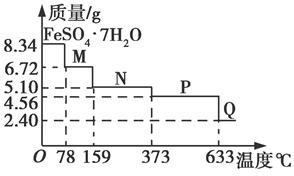
| A.温度为78℃时固体物质M的化学式为FeSO4·5H2O |
| B.温度为159℃时固体物质N的化学式为FeSO4·3H2O |
C.在隔绝空气条件下由N得到P的化学方程式为FeSO4 FeO+SO3↑ FeO+SO3↑ |
| D.取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3 |
下列说法中正确的是()
| A.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B.青铜是我国使用最早的合金,钢是用量最大、用途最广泛的合金 |
| C.漂白粉、漂粉精可用来漂白棉、麻、纸张,不能用作游泳池及环境的消毒剂 |
| D.合成纤维和光导纤维都是高分子化合物 |
1 L某混合溶液中,溶质X、Y的浓度都为0.1 mol/L,向混合溶液中滴加某溶液Z(0.1 mol/L的氢氧化钠或硫酸溶液),所得沉淀的物质的量随着Z溶液的体积变化关系如图所示,则X、Y、Z分别是()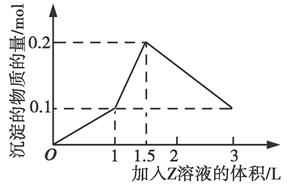
| A.AlCl3、FeCl3、NaOH |
| B.AlCl3、MgCl2、NaOH |
| C.NaAlO2、Ba(OH)2、H2SO4 |
| D.NaAlO2、BaCl2、H2SO4 |