在容积固定不变的密闭容器中加入1mol N2和3mol H2发生反应:N2(g)+3H2(g) 2NH3(g) △H=" —92.4" kJ·mol-1,下列结论正确的是
2NH3(g) △H=" —92.4" kJ·mol-1,下列结论正确的是
| A.该反应达到平衡时,放出的热量等于92.4kJ |
| B.达到平衡后向容器中通入1mol氦气,平衡不移动 |
| C.降低温度和缩小容器体积均可使该反应的平衡常数增大 |
| D.若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的90% |
可以验证硫元素的非金属性比氯元素弱的事实是
①H2S水溶液是弱酸,HCl水溶液是强酸
②向氢硫酸溶液中滴入氯水有单质硫生成
③硫、氯气分别与铁和铜反应,其产物是FeS、Cu2S、FeCl3、CuCl2
④高氯酸(HClO4)的酸性比硫酸强
| A.①②④ | B.②④ | C.②③④ | D.①②③④ |
某无色溶液,溶质仅由Na+、Ag+、Ba2+、Al3+、AlO2─、MnO4─、CO32─、SO42─中的若干种组成。取该溶液进行如下实验:
⑴取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液;
⑵在⑴所得溶液中加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;
⑶在⑵所得溶液中加入过量Ba(OH)2溶液并加热也有气体生成,同时析出白色沉淀乙。
则下列离子在原溶液中一定存在的有2
| A.SO42-、AlO2─、Na+、CO32─ | B.Na+、CO32─、AlO2─ |
| C.CO32─、Na+、Al3+ | D.MnO4─、Na+、CO32─ |
A、B、C、X均为中学化学常见物质,一定条件下它们有如下转化关系(其它产物已略去),下列说法错误的是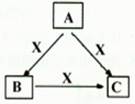
A、若X为Cl2,则C可能为FeCl3
B、若X为KOH溶液,则A可能为AlCl3
C、若X为O2,则A可为硫化氢
D、若A、B、C均为焰色反应呈黄色的物质,则X可能为O2
下列离子方程式正确的是
| A.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3+ + 2I- = 2Fe2+ + I2 |
| B.氧化铝溶解在NaOH溶液中:3H2O + Al2O3 + 2OH-= 2[Al(OH)4]- |
| C.硫酸铝溶液与氢氧化钡溶液反应,使SO42-恰好沉淀完全Al3+ + SO42-+ Ba2+ + 3OH- = BaSO4 ↓ + Al(OH)3↓ |
| D.在漂白粉配制成的溶液中通入SO2:Ca2+ + 2ClO- + SO2 + H2O = CaSO3↓+ 2HClO |
设NA为阿伏伽德罗常数的值。下列说正确的是
| A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA |
| B.室温下,1L pH=13的NaOH溶液中,由水电离的OH- 离子数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
| D.5NH4NO3= 2HNO3+ 4N2↑ + 9H2O反应中,生成28g N2时,转移的电子数目为3.75NA |