甲.乙.丙.丁四种易溶于水的物质,分别由NH4+.Ba2+.Mg2+.H+.OH-.Cl-.HCO3-.SO42-中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H+)>0.1mol/L;③ 向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论不正确的是( )
| A.甲溶液含有 Ba2+ | B.乙溶液含有SO42- |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |
下列涉及化学概念和进本原理说法正确的是
| A.12C14C C60互为同分异构体 |
| B.由同种元素组成的物质一定是纯净物 |
| C.金属氧化物存在酸性氧化物 |
| D.N2O3的水溶液能导电,说明N2O3是电解质 |
下列与摩尔盐[(NH4)2Fe(SO4)2.6H2O溶液有关离子方程式错误的是
| A.通入足量的溴水:2Fe2++Br2=2Fe3++2Br- |
| B.先加盐酸在通入BaCl2溶液:SO42-+Ba2+=BaSO4↓ |
| C.加氢氧化钠固体加热:NH4++OH-=NH3↑+H2O |
| D.检验该溶液是否变质:Fe3++3SCN-=Fe(SCN)3 |
化学反应条件(浓度、温度、加入实际量或顺序等)的变化会影响化学反应结果。下列对产生不同化学反应结果的影响因素分析错误的是
| 选项 |
反应物质 |
反应结果 |
影响因素 |
| A |
Na O2 |
Na2O Na2O2 |
反应温度 |
| B |
Cu HNO3 |
NO NO2 |
铜的还原性 |
| C |
Na2S溶液 SO2 |
澄清或者浑浊 |
SO2通入量 |
| D |
AgNO3 NH3.H2O |
澄清或者浑浊 |
试剂加入顺序 |
实验师模拟侯氏制碱法制取纯碱和氯化铵溶液,有关操作错误的是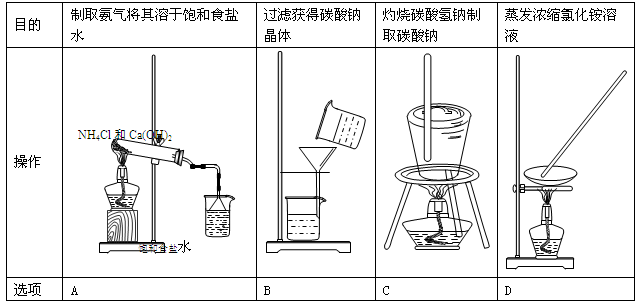
黑火药爆炸时可发生如下反应:5S+16KNO3+16C=3K2SO4+4K2CO3+K2S+12CO2↑+8N2↑,下列有关说法正确的是
| A.还原产物只有一种 |
| B.C即是氧化剂也是还原剂 |
| C.被氧化与被还原的S物质的量之比为3:1 |
| D.黑火药爆炸过程中对环境会造成污染 |