下表为长式周期表的一部分,其中的序号代表对应的元素。
(1)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为 杂化, 键与
键与 键的个数比为 。
键的个数比为 。
(2)元素③、④、⑤、⑥的第一电离能由大到小的顺序为 。其中⑥元素核外电子的电子排布图为 。
(3)③元素形成的最高价氧化物所形成的晶胞边长为acm,则其晶胞密度为 ;
(4)元素④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,还原产物没有气体,该反应的离子方程式为 。
(5)元素③与⑤形成的原子个数比为1:1化合物能与⑩的单质形成形式为A(BC)5的配合物,该配合物常温下为液态,易溶于非极性溶剂,其晶体类型 ,该配合物在一定条件下分解生成⑩的单质和③与⑤形成的原子个数比为1:1化合物,则在分解过程中破坏的化学键为 ,形成的化学键为 。
(6)化学上有一种见解,认为同种元素形成的含氧酸中该成酸元素的化合价越高,酸性越强,请用表中的元素举例说明(酸性由强到弱的顺序) 。
如图在下衬白纸的玻璃片中央放置适量的KmnO4颗粒,在周围分别滴加一滴KBr溶液,品红溶液,含有酚酞的澄清石 灰水,FeC12溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。
灰水,FeC12溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。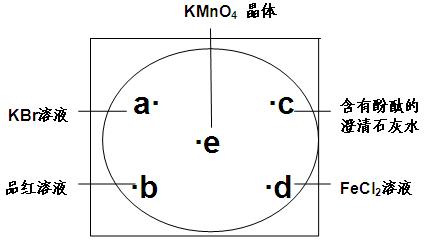
提示:实验室中所用的少量氯气可以用下述原理制取:
2KMnO4+16HC1(浓)2KC1+2MnC12+5C12↑+8H2O,此反应在常温下即能进行。
(1)a处反应离子方程式是。
(2)b处的现象是;d处的现象是。
(3)c处反应的化学反应在工业上用此原理制取漂白粉,在制取过程中用石灰乳而不用饱
和石灰水的原因是。
现有五种离子化合物A、B、C、D和E,都是由下表中离子形成的:
| 阳离子 |
Ag+ Ba2+ A13+ |
| 阴离子 |
OH- C1- SO42- |
为鉴别它们,分别完成以下实验,其结果是:
a.B和D都不溶于水,也不容于酸;
b.A溶于水后,与上述某阳离子反应可生成B,且A溶液与过量氨水反应生成白色沉淀;
c.C溶于水后,与上述某阳离子反应可生成D,且C溶液与过量氨水反应生成白色沉淀。
d.E溶于水后,与上述某阴离子反应可生成B;
e.A溶液与适量E溶液反应生成沉淀,再加入过量E溶液,沉淀量减少,但不消失。
请根据上述实验结果,填空:
(1)写出化合物的化 学式:A,C
学式:A,C ,
,
D,E。
(2)A溶液与过量的E溶液反应后,最终得到沉淀的化学式是。
已知“84消毒液”的有效成分是NaClO。试根据所学知识完成下列问题。
(1)试以食盐、水为原料,设计实验室制取“84消毒液”。(已知电解食盐水可得到氯气、氢氧化钠、水)
①实验内容为:电解食盐水制得氯气;
②实验内容为:;
反应方程式为:
③将制得的溶液装瓶保存。
(2)“84消毒液”的消毒原理是(用化学方程式表示)。用于杀死病菌的成分是(写化学式)。
(10分)有下列几个反应:①向NaAlO2溶液中滴加盐酸;②向盐酸和AlCl3的混合溶液中滴加NaOH溶液;③向NaOH溶液中滴加AlCl3溶液;
⑴符合反应①的图象是______,符合反应②的图象是_____,符合反应③的图象是____,(2)写出③步骤中的二个离子方程式__________________、________________________。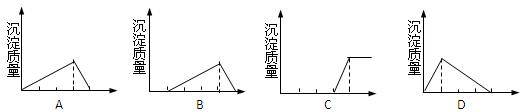
(4分)某可溶性盐的化学式XmYn(m≠n,X和Y不同时为弱电解质的对应离子),将一定量的该盐溶于适量的水中。
(1)若测得溶液的pH为3,则该盐与水反应的离子方程式___________________________;
(2)若该 盐水溶液的pH为11,则其与水反应的离子方程式为_______________________;
盐水溶液的pH为11,则其与水反应的离子方程式为_______________________;