下表对某些反应方程式的评价合理的是
| 编号 |
离子方程式或电极方程式 |
评价 |
|
| A |
Ca(ClO)2溶液中通入足量SO2 |
Ca2++ClO-+SO2+H2O=CaSO4+Cl-+2H+ |
正确 |
| B |
Ba(OH)2溶液中加入过量Al2(SO4)溶液 |
3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+Al(OH)3↓ |
正确 |
| C |
醋酸铵溶于水 |
CH3COO-+NH4+ CH3COOH+NH3·H2O CH3COOH+NH3·H2O |
错误,阴阳离子水解相互促进,应该用“=”号 |
| D |
用惰性电极电解 CuCl2 和NaCl的混合溶液一段时间 |
阴极:Cu2++2e-=Cu 阳极:4OH—4e-=2H2O+O2 |
错误,只因为两级得失电子没配平 |
向BaCl2溶液依次通入气体X和Y,下列各组不会出现沉淀的是
| 选项 |
X |
Y |
| A |
NH3 |
CO2 |
| B |
Cl2 |
CO2 |
| C |
SO2 |
NO2 |
| D |
Cl2 |
SO2 |
已知某强酸性的溶液中存在大量的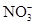 ,下列有关该溶液中还存在的物质叙述正确的是
,下列有关该溶液中还存在的物质叙述正确的是
A.铝元素能以Al3+或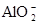 的形式存在 的形式存在 |
| B.铁元素能以Fe2+和Fe3+的形式共存 |
C.硫元素主要以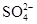 的形式存在 的形式存在 |
| D.氯元素能以Cl-或ClO-的形式存在 |
下列物质递变规律不能用元素周期律解释的是
| A.非金属性:C>Si |
| B.碱性:NaOH>Mg(OH)2 |
| C.酸性:H2SO3>H2CO3 |
| D.还原性:HI>HBr |
下列标志的高分子材料的单体,其中一种单体与其他三种单体均不是同系物的是
已知苯跟一卤代烷在催化剂作用下可生成苯的同系物。如: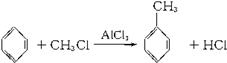
在催化剂作用下,由苯和下列各组物质合成乙苯最好应选用的是:
| A.CH3—CH3和Cl2 | B.CH2=CH2和Cl2 |
| C.CH2=CH2和HCl | D.CH≡CH和Cl2 |