下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
在Ba(NO3)2溶液中分别滴入H2SO3及H2SO4溶液 |
均有白色沉淀 |
沉淀均为BaSO4 |
| B |
混合装有Cl2和NH3量集气瓶中的气体 |
产生大量白烟 |
NH3显还原性和碱性 |
| C |
溶液X中滴入盐酸酸化的FeCl2溶液,再滴入淀粉溶液 |
溶液变蓝色 |
溶液X中一定含有I- |
| D |
向浓度居委0.01mol/LNaCl和Na2S的混合溶液中滴入少量AgNO3 |
出现黑色沉淀 |
Ksp(Ag2S)>Ksp(AgCl) |
在一定条件下,反应N2+3H2 2NH3在10L密闭容器中进行,测得2min内,N2的物质的量由6mol减少到2mol,则2min内N2的平均反应速率为()
2NH3在10L密闭容器中进行,测得2min内,N2的物质的量由6mol减少到2mol,则2min内N2的平均反应速率为()
| A.0.4 mol/(L·min) | B.0.2 mol/(L·min) | C.0.3 mol/(L·min) | D.0.6mol/(L·min) |
下列离子方程式书写正确的是()
| A.锌和稀硝酸反应:Zn+2H+=Zn2++H2↑ |
| B.碳酸钡和盐酸反应:CO32-+2H+=CO2↑+H2O |
| C.三氯化铝加到过量的氨水中:Al3++3OH-=Al(OH)3↓ |
| D.氯气通入氢氧化钾溶液中:Cl2+2OH-=Cl-+ClO-+H2O |
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生气泡的是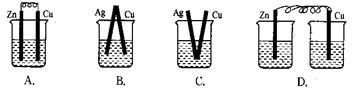
以下分离或提纯的方法中正确的是()
| A.分离碘水中的碘——升华 | B.分离白酒中的酒精和水——分液 |
| C.除去海盐中的硫酸盐——溶解后加硝酸钡 | D.分离海水中的水——蒸馏 |
下列溶液中的Cl-浓度与50 mL 1 mol ·L-1 MgCl2溶液中的Cl-浓度相等的是()
| A.150 mL 1 mol·L-1 NaCl溶液 | B.75 mL 0.5mol·L-1CaCl2溶液 |
| C.150 mL 2 mol·L-1 KCl溶液 | D.75 mL 1 mol ·L-1AlCl3溶液 |