已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E元素是第四周期元素中未成对电子数最多的元素,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol配合物与足量的AgNO3溶液反应能立即生成3molAgCl。F原子的一种核素的质量数为65,中子数为 36。请根据以上情况,回答下列问题:(答题时要用元素符号表示)
(1)B氢化物与HCl反应生成的含有B元素粒子的空间构型是 .F元素原子的最外层电子数为 个。
(2)B3-离子分别与AC2、由B、C组成的气态化合物互为等电子体,则B、C组成的化合物化学式为 ;B3-离子还可以和一价阴离子互为等电子体,这阴离子电子式为 ,这种阴离子常用于检验日常生活中的一种金属阳离子,这金属阳离子符号为
(3)A、B、C的第一电离能由小到大的顺序为
(4)E3+的核外电子排布式是 ,ECl3形成的六配位的配合物化学式为 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
(6)在F的+1价氧化物的晶胞结构如图,F为 球(“黑”“白”)
有A、B、C、D四种无色溶液,它们分别是Na2CO3、Na2SO4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为::①A+D→溶液+气体,②B+C→溶液+沉淀,
③B+A→溶液+沉淀X,④D+B→溶液Y+沉淀,⑤溶液Y+沉淀X→溶液+气体.
(1)根据以上记录确定:A__________ B___________ C___________ D___________
(2)写出①、③各反应的离子方程式:
①_______________③______________
有甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、CO32-、SO42-中的不同阴、阳离子各一种组成,已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)它们的化学式分别为甲_________、乙_________、丁_________。
(2)写出甲溶液和丁溶液反应的离子方程式:_________________________。
(3)检验乙中阴离子所用试剂的名称是____________________。
1mol仅含C、H、O三种元素的有机物A在稀硫酸中水解生成1molB和1molC,B分子中N(C):N(H)=4:5,135<Mr(B)<140;C与B分子中C原子数相同,且:Mr(B)=Mr(C)+2.(N代表原子个数,Mr代表相对原子质量)
(1)C的分子式为_______________,A的摩尔质量为______________;
(2)B的分子具有高度对称性,苯环上的一氯取代物只有一种.B能与金属Na反应但不能与NaOH反应.写出B的结构简式______________;
(3)C有多种同分异构体,其中属于芳香酯类的同分异构体有__________种,写出其中一种的结构简式____________;
(4)C分子中苯环上有两个取代基,且苯环上的一氯取代物有两种.写出A的结构简式______________。
由乙烯和其他无机原料合成环状酯,其合成过程如下(水及其他无机产物均已省略)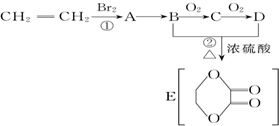
请分析后回答下列问题:
(1)写出下列反应的反应类型:①______________;②______________;
(2)D物质中的官能团名称为______________;
(3)物质X与A互为同分异构体,则X的结构简式为______________;
(4)写出下列转化的化学方程式:A→B______________;
B+D→______________。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X的原子结构示意图为________________ Y原子核外价电子排布图 ________________。
(2)XZ2与YZ2分子的立体结构分别是________和________________,相同条件下两者在水中的溶解度较大的是__________(写分子式),理由是_________________________。
(3)Q的元素符号是__________,它的基态原子的核外电子排布式为______________,在形成化合物时它的最高化合价为__________。
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键_____________________。