一定量的锌与100mL18.5mol•L﹣1的浓H2SO4充分反应后,锌完全溶解,同时生成标准状况下的气体33.6L.将反应后的溶液稀释至1L,测得溶液中c(H+)=0.1mol•L﹣1.则生成的气体中SO2和H2的体积比为( )
| A.1:2 | B.2:1 | C.1:4 | D.4:1 |
某溶液中存在XO3―,且X为短周期元素,则一定能在该溶液中大量共存的离子组是()
| A.Na+ H+ SO42― I― | B.Na+ Ca2+ CO32― Al3+ |
| C.Na+ K+ Fe2+ H+ | D.K+ SO42― Cl― CO32― |
今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是( )
A.若a=b,且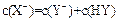 ,则相同条件时,酸性 ,则相同条件时,酸性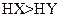 |
B.若a=b,且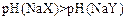 ,则相同条件时,酸性 ,则相同条件时,酸性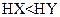 |
C.若a>b,且 ,则相同条件时,酸性HX<HY ,则相同条件时,酸性HX<HY |
D.若等体积混合,且 ,则一定有 ,则一定有 |
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2 = LiNH2+ LiH下列说法正确的是()
| A.亚氨基锂(Li2NH)中N的化合价为-1 |
| B.此法储氢和钢瓶储氢的原理相同 |
| C.Li+ 和H— 的半径相同 |
| D.该反应中氢气既是氧化剂又是还原剂 |
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是()
| A.25℃时,1 L pH=13的NaOH溶液中约含有6.02×1023个氢氧根离子 |
| B.1L 1 mol·L-1的盐酸中,所含氯化氢分子数为6.02×1023 |
| C.1 mol羟基(-OH)所含的电子数约为10×6.02×1023 |
| D.标准状况下,一定量的铜与硝酸反应后生成22.4 L NO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于6.02×1023 |
对于氯化铁溶液和氢氧化铁胶体,以下说法正确的是()
| A.分散质粒子直径都在1nm~100nm之间 |
| B.分散质微粒都能透过半透膜 |
| C.加热蒸干并灼烧后都有氧化铁生成 |
| D.分散系中分散质微粒前者带电荷、后者不带电荷 |