电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧—钠氧化法”回收Na2Cr2O7等物质。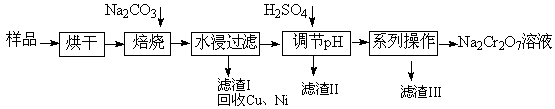
已知:水浸后溶液中存在Na2CrO4、NaAlO2[也可表示为NaAl(OH)4]、Na2ZnO2等物质。
(1)水浸后回收Cu、Ni时的操作是 。水浸后的溶液呈 性(“酸”、“碱”、“中”)
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式
Cr(OH)3 + Na2CO3 + O2 Na2CrO4 + CO2 + H2O
Na2CrO4 + CO2 + H2O
(3)滤渣II的主要成分有Zn(OH)2、 。
(4)已知:①除去滤渣II后,溶液中存在如下反应:CrO42—+ 2H+ Cr2O72—+ H2O;②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
Cr2O72—+ H2O;②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
| 化学式 |
20℃ |
60℃ |
100℃ |
| Na2SO4 |
19.5 |
45.3 |
42.5 |
| Na2Cr2O7 |
183 |
269 |
415 |
| Na2CrO4 |
84 |
115 |
126 |
“系列操作”中为:继续加入H2SO4, 冷却结晶,过滤。继续加入H2SO4目的是__________________________________________________。
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨做电极电解生产金属铬,写出生成铬的电极反应方程式 。