工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,已知该反应分为两步进行,第一步为2ClO3- + 2Cl- + 4H+ = 2ClO2↑+ Cl2↑+ 2H2O。
(1)写出第二步反应的离子方程式 。
(2)工业生产时需在反应物中加少量Cl-,其作用是 。
(3)生产中会发生副反应ClO3- + Cl- + H+ - Cl2↑+ H2O(未配平),若测得反应后的混合气体中Cl2的体积分数为3/73,则起始投料时CH3OH与NaClO3的物质的量之比为 。
(写出解题过程)
下列物质的水溶液能导电且属于非电解质的是
| A.酒精 | B.Cl2 | C.S02 | D.NH4N03 |
在给定条件下,可以大量共存的离子组是
| A.含有0.1 mol·L—1 Fe3+的溶液中:H+、Fe2+、Na+、Br- |
B.强碱性溶液中:K+、Al3+、Cl—、SO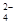 |
| C.在pH=1的溶液中:Mg2+、Na+、ClO-、NO3- |
| D.加入强碱再加热,既有气体放出又有沉淀生成的溶液:Ca2+、HCO3-、NH4+、Cl- |
下列实验过程中,始终无明显现象的是
| A.NO2通人FeSO4溶液中 | B.CO2通入CaCl2溶液中 |
| C.NH3通入AlCl3溶液中 | D.SO2通入已酸化的Ba(NO3)2溶液中 |
用100 mL 10 mol·L-1的浓盐酸与足量的MnO2共热,充分反应后,被氧化的HCl的物质的量
| A.小于0.5 mol | B.等于0.5 mol |
| C.在0.5~1.0 mol之间 | D.大于0.5 mol |
将盛有NO2和O2的混合气体的试管倒扣在水中,充分反应后,试管内充满溶液,则NO2和O2的体积比为
| A.1:1 | B.3:1 | C.4:3 | D.4:1 |