下列离子方程式正确的是
| A.用氢氧化钠溶液除去铝片表而上的氧化膜:Al3++4OH-=AlO2-+2H2O |
| B.在含3.2amolHNO3的稀溶液中,加入amol铁粉:5Fe+4NO3-+16H+=3Fe2++2Fe3++4NO↑+8H2O |
| C.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D.过氧化氢能使酸性KMnO4溶液褪色:3H2O2+2MnO4-+6H+=2Mn2++4O2↑+6H2O |
在密闭容器中将CO和水蒸气的混合物加热到800℃时,有下列平衡:CO+H2O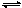 CO2+H2,且K=1。若用2molCO和10mol H2O相互混合并加热到800℃,则CO的转化率为
CO2+H2,且K=1。若用2molCO和10mol H2O相互混合并加热到800℃,则CO的转化率为
| A.16.7% | B.50% |
| C.66.7% | D.83.3% |
一定温度下,有可逆反应:2A(g)+2B(g)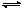 C(g)+3D(g)ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g)ΔH<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
关于两容器中反应的说法正确的是
| A.甲容器中的反应先达到化学平衡状态 |
| B.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示 |
| C.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同 |
| D.在甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度与乙中物质C的浓度相等 |
可逆反应:2NO2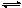 2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中进行,达到平衡状态的标志是
①单位时间内生成nmolO2的同时生成2nmolNO
②单位时间内生成nmolO2的同时生成2nmolNO2
③用NO2,NO,O2表示的反应速率的比为2∶2∶1的状态
④混合气体的压强不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
⑦混合气体的颜色不再改变的状态
| A.②④⑥⑦ | B.②③⑤⑦ |
| C.①③④⑤ | D.全部 |
某温度下,向2L恒容密闭容器中充入1.0molA和1.0molB,反应A(g)+B(g)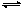 C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
| t/s |
0 |
5 |
15 |
25 |
35 |
| n(A)/mol |
1.0 |
0.85 |
0.81 |
0.80 |
0.80 |
A.反应在前5 s的平均速率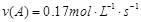
B.保持其他条件不变,升高温度,平衡时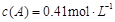 ,则反应的
,则反应的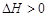
C.相同温度下,起始时向容器中充入0.20molA、0.20molB和1. 0molC,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0 molC达到平衡时,C的转化率小于80%
在一定体积的密闭容器中进行反应:N2(g)+3H2(g) 2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L,0.3mol/L,0.2mol/L。当反应达到平衡时,可能存在的数据是
2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L,0.3mol/L,0.2mol/L。当反应达到平衡时,可能存在的数据是
| A.N2为0.2mol·L-1,H2为0.6mol·L-1 |
| B.N2为0.15mol·L-1 |
| C.N2、H2均为0.18mol·L-1 |
| D.NH3为0.4mol·L-1 |