某化学兴趣小组拟采用下图所示装置电解饱和氯化钠溶液制备H2,通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu),同时检验Cl2的氧化性(图中夹持和加热仪器已略去)。
(1)直流电源中的X极为 极(填“正”、“负”、“阴”或“阳”);写出甲装置U形管中反应的离子方程式: ;实验开始后,用铁棒作电极的一侧的实验现象是 。
(2)为完成上述实验,正确的链接顺序为:a连 ,b连 (填写连接的字母)。
(3)装置乙中的G瓶内溶液可能为 (填字母)。
| A.淀粉KI溶液 | B.NaOH溶液 | C.Na2S溶液 | D.Na2SO3溶液 |
H瓶内的反应的离子方程式为: 。
(4)在对硬质玻璃试管里的氧化铜粉末加热前需要进行的操作为: 。
(5)装置丙中N瓶内盛放的试剂为 ,作用是 。
(6)为了测定Cu的相对原子质量,某同学通过实验测得如一下数据:
I.氧化铜样品质量为m1g
Ⅱ.反应后硬质玻璃管中剩余固体质量为m2g
Ⅲ.反应前后U形管及其固体质量差为m3g
Ⅳ.反应前后瓶及其液体质量差为m4g
①请选择理论上误差最小的一组数据计算Ar(Cu),Ar(Cu)= 。
②如果选用其它数据进行计算,会导致Ar(Cu) (填“偏大”、“偏小”或“无影响”),理由是 。
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
【探究一】设计如图所示装置进行“铁与水反应”的实验。
(1)硬质玻璃管中发生反应的化学方程式为______________________________。
(2)反应前A中投放碎瓷片的目的是____________________________________。
(3)装置E中的现象是________________________________________________。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于_______后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同)为_______;若溶液未变红色,推断硬质玻璃管B中固体物质的成分为_______。
①一定有Fe3O4②一定有Fe
③只有Fe3O4④只有Fe
(6)另一份用_______(填仪器名称)加入_______,可以证明溶液中存在Fe2+。
【探究三】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
(7)试剂b的化学式是_______。
(8)计算反应后B装置中铁元素的质量分数为_______。
一般测定样品中成分含量的实验应重复2~3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:
Ⅰ.甲同学的方案如图所示:
(1)如何检验A装置的气密性?_____________________________________________。
(2)甲同学重复进行了三次实验,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能引起测量结果偏低的原因是_______(填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收
D.加入稀硫酸的量不足、反应不充分
(3)为了让甲的实验测量结果更准确,在其他实验步骤都正确的条件下,你认为图中的实验装置应该如何改进:______________。
Ⅱ.乙同学的方案是:从图中所提供的装置中选择实验装置,代替甲同学实验装置中的B、C,通过测定放出的二氧化碳的体积(不考虑二氧化碳溶于水)来计算。
选择最简装置的连接顺序为_______。
Ⅲ.丙同学的方案是:称取样品m g,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体n g。
(1)配制100 mL 0.10 mol/L BaCl2溶液的实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外还有_______(填仪器名称)。
(2)混合物中碳酸钠的质量分数为(用m、n表示)_______。
(3)Ca2+、Ba2+都可以使 沉淀完全,能否使用氯化钙溶液代替氯化钡溶液?_______ (填“能”或“否”),原因是:_____________________________________。
沉淀完全,能否使用氯化钙溶液代替氯化钡溶液?_______ (填“能”或“否”),原因是:_____________________________________。
如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
(1)该实验的实验目的是__________________________________________。
(2)在A试管内发生反应的化学方程式是_______________________________。
(3)B装置的作用是_________________________________________________。
(4)在双球干燥管内发生反应的化学方程式为____________________________。
(5)实验时观察到的实验现象是_______________________________________。
上述实验现象说明___________________________________________________。
(6)若将干燥管内的Na2O2换成Na2O,则实验时观察到的实验现象是___________。
某研究性学习小组欲利用已经学过的化学知识和下列装置制取少量次氯酸钠,并进一步探究次氯酸钠的化学性质。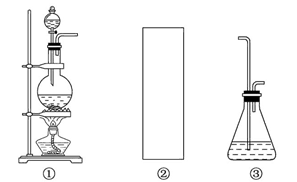
相关资料:反应Cl2+2NaOH=NaClO+NaCl+H2O属于放热反应,温度稍高时便发生副反应:3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
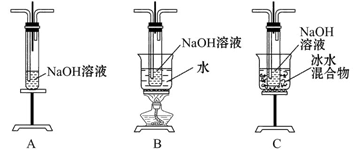
(1)制取氯气时,在烧瓶中加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。请在装置A、B、C中选择一个合适的装置放在②处________。
(2)部分学生认为上述装置存在缺点,他们指出在前两个仪器之间应增加如D图所示的装置:你认为D中所盛液体是________,其作用是____________。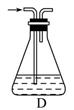
(3)该化学兴趣小组对产品的性质进行了如下探究。
第一步,测其pH=10。结合相关离子方程式解释原因________。
第二步,该化学兴趣小组的同学备选了紫色石蕊试液对次氯酸钠的性质进行实验检验。请你帮助他们完成实验报告:
| 实验操作 |
预期现象 |
结论 |
CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物(如FeS等)。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。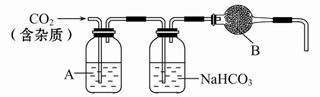
完成下列填空:
(1)用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1),应选用的仪器是_____。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是_____溶液,NaHCO3溶液可以吸收_____。
(3)上述装置中,B物质是_____。把这个实验得到的气体收集起来,用来测定CO2的分子量,如果B物质失效,测定结果_____(填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重,为了将石蜡溶出,应选用的试剂是_____,碳酸钙溶出,应选用的试剂是_____。
a.氯化钠溶液 b.稀醋酸
c.稀硫酸 d.正己烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出_____,原因是_______________。