铁及其化合物在生活生产中有重要的应用。请回答下列问题:
(1)在盛有氧气的集气瓶中点燃细铁丝发生剧烈燃烧的化学方程式是
(2)已知铁能与氯化铁反应生成氯化亚铁。将生锈的铁钉(铁锈的主要成分是
)放入盐酸中,充分反应后有铁剩余,写出发生置换反应的化学方程式
(3)高炉炼铁中,焦炭的作用是
(4)把铁粉和铜粉的混合物放入硝酸银溶液中,反应结束后有固体剩余。下列说法正确的是
如图为A、B、C三种物质的溶解度曲线。请据图回答: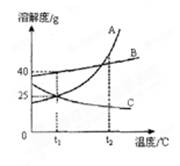
(1)要使接近饱和的C溶液变为饱和溶液,可采用的一种措施是;
(2)t2℃时,将等质量的A、B、C三种物质的饱和溶液同时降温至t1℃,析出晶体最多的是所得溶液中溶质质量分数最小的是
下表是一些烷烃的物理常数,请根据下表回答:
| 一些链烷烃的物理常数 |
||||
| 名称 |
分子式 |
沸点/℃ |
熔点/℃ |
相对密度 |
| 甲烷 |
CH4 |
-161.7 |
-182.6 |
—— |
| 乙烷 |
C2H6 |
-88.6 |
-172.0 |
—— |
| 丙烷 |
C3H8 |
-42.2 |
-187.1 |
0.5005 |
| 丁烷 |
C4H10 |
-0.5 |
-135.0 |
0.5788 |
| 戊烷 |
C5H12 |
36.1 |
-129.3 |
0.6264 |
(1)请根据上表找出两条规律,。
(2)分析上表写出常温下是气态的烷烃。
下面是普通电池中发生的反应:
Zn+2MnO2+2NH4Cl===ZnCl2+Mn2O3+2NH3+H2O
(1)该反应中,Zn的化合价由变为。
(2)将该反应中的反应物进行简单分类,在下面横线上的物质是(填名称)
单质:_____________;
金属氧化物:_____________。
小强准备用锌和稀硫酸制取氢气,可是实验室只有98%的浓硫酸,于是小强用100ml量筒量取5ml的浓硫酸,准备在量筒里加水稀释,小刚见了马上制止了小强的操作,请指出上述已完成和未完成的操作中:
(1)存在的错误有,,。
(2)可能造成的后果有。
(3)反应原理用化学方程式表示为。
(4)如果把稀硫酸改为稀盐酸与锌粒反应制取氢气,你认为不足之处是。
如图是A、B固体物质的溶解度曲线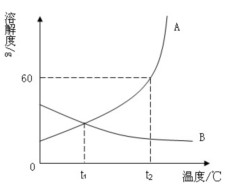
(1)在时两种物质的溶解度相同。
(2)t1℃时分别将两种物质等质量的饱和溶液降温到0℃,溶液中溶质的质量分数是AB(填“大于”“小于”“等于”)。
(3)t2℃时向70g甲物质中加入100g水,充分溶解后,所得溶液(填“是”“不是”)饱和溶液,该溶液的溶质的质量是。