运用化学反应原理研究氮、碳、硫等单质及其化合物的反应有重要意义。
(1)氨在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量。
①若起始时向容器内放入2mol N2和6mol H2,达平衡后放出的热量为Q,则Q(填 “>”、“<”或“=”) 184.4 kJ。
②已知
1mol N—H键断裂吸收的能量等于 kJ。
(2)硫酸的年产量可以用来衡量一个国家的化工生产能力。工业生产硫酸的流程中存在反应:2SO2(g)+O2(g) 2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g)。反应体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题: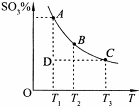
①该反应的 0(填“>’或“<”)。
0(填“>’或“<”)。
②下列说法正确的是
a.若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡不移动
b.在D点时,v正>v逆
c.B点、C点反应的平衡常数分别为K1、K2,则K1<K2
d.在A点时,消耗1mol SO2必定同时消耗1mol SO3
(3)过度排放CO2会造成温室效应。
①最近科学家提出“绿色自由”构想能把空气中的CO2转变为可再生燃料甲醇。甲醇可制作燃料电池,写出该电池负极反应式(电解液为KOH溶液) 。
②CO2也可用NaOH溶液吸收得到Na2CO3溶液,写出该反应的离子方程式 。
Na2CO3水溶液呈碱性,其原因是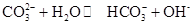 ,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。
,25℃时该反应的K=2×10-4mol·L-1,则当溶液中c(HCO- 3):c(CO2- 3)=2∶1时,溶液的pH= 。
某炼铁厂在冶炼生铁过程中,矿石中的铁有2%损耗掉,该厂每天生产含铁95%的生铁70t,问需含Fe2O370%的赤铁矿多少吨?
在长期的生产实践中,人类对各种金属器件的防锈问题已找到一些理想的措施,例如:
(1)农机具采用;
(2)地下输油管道采用;
(3)远洋巨轮船体采用;
(4)大型水库的钢铁闸门采用。
铁是自然界里分布最广的金属元素之一,在地壳中的质量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是Fe2O3)等。
(1)写出用赤铁矿石炼铁的主要化学反应方程式。
(2)红热的铁能跟水蒸气起反应,有一种产物是可燃性气体,则其反应的化学方程式为。在常温下,铁跟水不反应,但是,在水和空气里的氧气及二氧化碳等的共同作用下,铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁产量的四分之一。刷油漆是重要的防腐蚀措施之一,油漆防腐蚀的主要原理是。
(3)铁元素是人体的重要营养元素,举一例说明铁元素在人体中的重要作用。
已知有关物质的熔沸点数据如下表:
| MgO |
Al2O3 |
MgCl2 |
AlCl3 |
|
| 熔点/℃ |
2852 |
2072 |
714 |
190 |
| 沸点/℃ |
3600 |
2980 |
1412 |
182.7 |
请参考上述数据填空和回答问题。
(1)工业上常用电解熔融MgCl2的方法生产金属镁,而不用电解电解MgO的方法生产镁。
(2)工业上用电解Al2O3与冰晶石熔融混合物的方法生产铝,而不用电解AlCl3的方法生产铝,冰晶石在炼铝过程中的作用是。
(1)炼钢和炼铁都利用氧化还原反应,但炼铁是有,其核心反应是。而炼钢主要是用,其除碳的反应为。
(2)炼铁时常用的焦炭形成还原剂,能用煤代替吗?,为什么?
(3)检查钢质设备完好性的方法之一是:在被怀疑有裂纹处涂上10%的盐酸,过一段时间如观察到有粗线裂纹,表明该部分原先确有裂纹,产生粗线裂纹的原因是