下列有关化学概念或原理的论述中,正确的是
| A.Cl2、SO2、NH3的水溶液都能够导电,因此都属于电解质 |
| B.任何一个氧化还原反应都可以设计为电池,输出电能 |
| C.任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大 |
| D.电解饱和食盐水的过程中,水的电离平衡正向移动 |
已知25℃时,弱电解质的电离平衡常数:Ka(CH3COOH)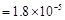 ,Ka(HSCN)
,Ka(HSCN)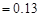 。在物质的量浓度均为
。在物质的量浓度均为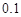 mol·L
mol·L 的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
A.c(OH )>c(CH3COOH)>c(HSCN)>c(H )>c(CH3COOH)>c(HSCN)>c(H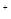 ) ) |
B.c(OH )>c(HSCN)>c(CH3COOH)>c(H )>c(HSCN)>c(CH3COOH)>c(H ) ) |
C.c(OH )>c(SCN )>c(SCN )>c(CH3COO )>c(CH3COO )>c(H )>c(H ) ) |
D.c(OH )>c(CH3COO )>c(CH3COO )>c(SCN )>c(SCN )>c(H )>c(H ) ) |
气体制备装置中不能“随开随制,随关随停”的是( )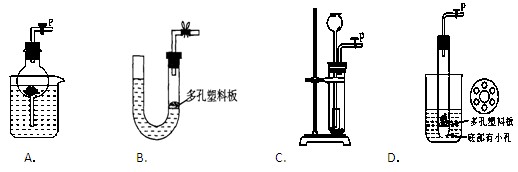
一定量的氢气在氯气中燃烧,所得混合物冷却后用500mL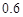 mol·L
mol·L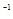 的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为
的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为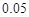 mol,参加反应的氢气和所用氯气的物质的量之比为( )
mol,参加反应的氢气和所用氯气的物质的量之比为( )
A.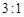 |
B.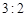 |
C. |
D.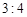 |
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体可能是( )
① CO、O2 ② Cl2、CH4 ③ NO2、O2 ④ N2、H2
| A.①② | B.②④ | C.③④ | D.②③ |
双氧水可作为采矿业废液的处理剂,如用来消除采矿废液中的氰化物,反应方程式如下:KCN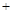 H2O2
H2O2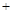 H2O → A
H2O → A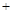 NH3↑。下列说法正确的是( )
NH3↑。下列说法正确的是( )
| A.生成物A是一种正盐 | B.氨气是还原产物 |
| C.该反应中H2O2作氧化剂 | D.处理 mol KCN转移 mol KCN转移 mol电子 mol电子 |