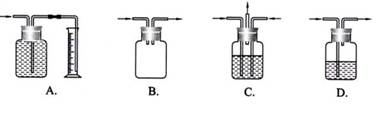
常温下,向20.00 mL 0.100 mol/LCH3COONa溶液中逐滴加入0.1 000 mol/L盐酸,溶液的pH与所加盐酸体积的关系如右下图所示(不考虑挥发)。下列说法正确的是

绿原酸的结构简式如图,下列有关绿原酸的说法不正确的是
| A.分子式为C16H18O9 |
| B.能与Na2CO3反应 |
| C.能发生取代反应和消去反应 |
| D.0.1 mol绿原酸最多与0.8 mol NaOH反应 |
下列有关化学用语表示正确的是
A.比例模型 可以表示水分子,也可以表示二氧化碳分子 可以表示水分子,也可以表示二氧化碳分子 |
B.电子式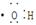 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
C.离子结构示意图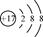 可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- |
D.离子方程式HCO3-+H2O H3O+ +CO32-可以表示HCO3-离子的水解,也可以表示它的电离 H3O+ +CO32-可以表示HCO3-离子的水解,也可以表示它的电离 |
下列解释实验事实的反应方程式不正确的是
| A.盛放烧碱的试剂瓶不能用玻璃塞:SiO2+2NaOH=Na2SiO3+H2O |
| B.用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O |
C.用KSCN溶液检验Fe3+:Fe3++3SCN- Fe(SCN)3 Fe(SCN)3 |
| D.酸性KI淀粉溶液久置后变蓝:4I-+O2+2H2O=2I2+4OH- |
下列说法正确的是
| A.4.2 g丙烯中所含的共价键数目为0.6×6.02×1023 |
| B.含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为6.02×1023 |
| C.相同条件下,1 L CO和H2的混合气体完全燃烧消耗0.5 L O2 |
| D.相同物质的量OH-和CH3+含有相同数目的电子 |
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其它简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是