下列说法正确的是
| A.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| B.浓度均为0.1mol·L-1的下列溶液,pH由大到小排列顺序为NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
| C.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比为1:2 |
| D.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
下列有机物命名正确的是()
| A.2, 4,4-三甲基戊烷 | B.2-乙基丁烷 |
| C.2, 2,3, 4-四甲基戊烷 | D.3, 4,4-三甲基戊烷 |
某溶液中加入铝片有氢气产生,则该溶液中一定能大量共存的离子组是
| A.Cl― NO3― Ba2+ Fe3+ | B.SO42― S2― Al3+ Mg2+ |
| C.Na+ K+ SO42― Cl― | D.NH4+ Ba2+ Cl― HCO3― |
下列装置所示的实验不能达到目的的是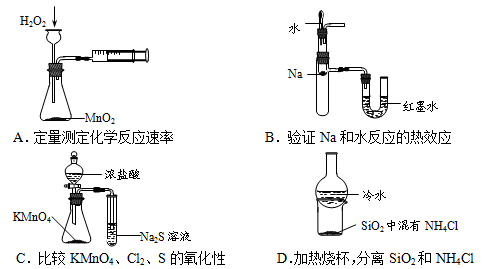
下列有关铁元素的叙述中正确的是()
| A.Fe(OH)2易被氧化生成Fe(OH)3,说明稳定性:Fe(OH)2<Fe(OH)3 |
| B.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| C.氢氧化铁与氢碘酸反应:Fe(OH)3+3HI→FeI3+3H2O |
| D.铁元素位于周期表的第五周期第VIII族 |
短周期元素aA2+、bB+、cC3-、dD-都具有相同电子层结构,则下列叙述正确的是()
| A.原子半径A>B>D>C | B.原子序数D>C>B>A |
| C.离子半径C>D>B>A | D.单质还原性A>B>D>C |