近年来,以天然气等为原料合成甲醇的难题被一一攻克,极大地促进了甲醇化学的发展。
(1)与炭和水蒸气的反应相似,以天然气为原料也可以制得CO和H2,该反应的化学方程式为_________。
(2)合成甲醇的一种方法是以CO和H2为原料,其能量变化如图所示:
由图可知,合成甲醇的热化学方程式为________________________________________。
(3)以CO2为原料也可以合成甲醇,其反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
①在lL的密闭容器中,充入1molCO2和3molH2,在500℃下发生反应,测得CO2(g)和CH3OH(g)的浓度随时问变化如图所示:
则下列说法正确的是_________________(填字母);
| A.3min时反应达到平衡 |
| B.0~10min时用H2表示的反应速率为0.225mol·-1·min-1 |
| C.CO2的平衡转化率为25% |
D.该温度时化学平衡常数为 (mol/L)-2 (mol/L)-2 |
②在相同温度、相同容积的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 |
容器1 |
容器2 |
容器3 |
| 反应物投入量(始态) |
1molCO2、3molH2 |
0.5molCO2、1.5molH2 |
1molCH3OH、1molH2O |
| CH3OH的平衡浓度/mol•L-1 |
c1 |
c2 |
c3 |
| 平衡时体系压强/Pa |
p1 |
p2 |
p3 |
则下列各量的大小关系为c1___________c3,p2_________p3(填“大于”、“等于”或“小于”)。
(4)近年来,甲醇燃料电池技术获得了新的突破,如图所示为甲醇燃料电池的装置示意图。电池工作时,分别从b、c充入CH3OH、O2,回答下列问题:
①从d处排出的物质是___________,溶液中的质子移向电极__________(填“M”或“N”);
②电极M上发生的电极反应式为__________________________。
(4分) 标准状况下,1.12LCH4和C2H4的混合气体缓慢通入足量溴水中,溴水增重0.28g,则乙烯占混合气体的体积分数为:。
将等物质的量的A、B混合于1 L的密闭容器中,发生如下反应
3A(g)+B(g) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)=n(B)=________mol。
(2)B的平均反应速率v(B)=________mol/(L·min)。
(3)x的值为________。
在4L的密闭容器中,充入1molN2和4molH2,在一定条件下反应,3分钟后达到平衡状态,相同温度下,测得平衡时气体的压强比反应前混合气体的压强减少了12%,则
(1)平衡时混合气体中三种气体的物质的量之比为。
(2)N2的转化率为。
(3)3分钟内NH3的平均反应速率为。
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。
⑴通过计算推测:
①原混合溶液NaCl和CuSO4的物质的量浓度。
②t2时所得溶液中氢离子物质的量浓度
⑵实验中发现,阳极产生的气体体积与阴极相比,明显小于对应时间段的理论值。试简要分析其可能原因。
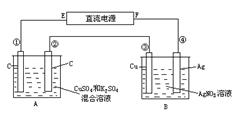
如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL,求通电前A池中原混合溶液Cu2+的浓度。