氢化钙(
)固体是登山队员常用的能源提供剂.某化学兴趣小组拟用如图1所示的装置制备氢化钙,其反应的化学方程式为:
.

(1)
中钙和氢元素的化合价分别为
(2)利用该装置进行实验,步骤如下:检查装置的气密性后装入药品,打开分液漏斗活塞:
①加热反应一段时间 ②收集气体并检验其纯度 ③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)为了确认进入装置C的氢气已经干燥,应在B、C之间再连接一装置
,装置
中加入的试剂是
(4)为了测量上述实验中制得的氢化钙的纯度,该小组称取mg所制得样品,按如图2所示装置进行测定.旋开分液漏斗活塞,反应结束后充分冷却,注射器活塞由反应前的V1mL刻度处变化到V2mL刻度处(V2<V1,气体密度为dg/mL)
①橡胶管的作用为:a
②旋开分液漏斗活塞后,除发生
的反应外,还最有可能发生的反应为
③用w表示氢化钙的纯度,请用一个等式表示出d、V1、V2和w之间的关系
④该小组乙同学认为去掉连接的注射器,也要计算出氢化钙的纯度.他同样称取mg样品,加入烧瓶中后称取反应前的质量为m1g,反应后的质量为m2g.乙同学表示出的m,m1,m2和w之间的关系的等式为
为了测定某赤铁矿石中氧化铁的质量分数,取矿石样品40g,加入盐酸,恰好完全反应时,共用去盐酸219g,过滤、洗涤、干燥后得滤渣8g(矿石中的杂质既不溶于水也不与盐酸反应)。计算:
(1)赤铁矿石中氧化铁的质量分数;
(2)盐酸的溶质质量分数。
某校学习小组测定酸碱中和反应。他们向50g 8%的氢氧化钠溶液中加入100g的稀盐酸恰好完全反应,此时溶液PH=7。请你帮他们计算:所用稀盐酸溶质的质量分数是多少?
化学兴趣小组的同学取10 g某锌样品(含少量杂质,且杂质不溶于水,也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸的质量为93.7 g时,恰好完全反应,生成气体的质量与反应时间的关系如下图所示,试回答下列问题: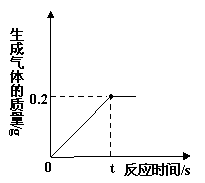
(1)从图中可以看出,完全反应后生成氢气的质量为g。
(2)样品中锌的质量为多少?(3)反应后,所得溶液中硫酸锌的质量分数为多少?
媒体近日报道:市面上部分方便面遭到塑化剂污染,长期接触塑化剂可引起血液系统、生殖系统损害,其中,塑化剂(DMP)分子式为C10H10O4。求:
(1)DMP的相对分子质量为_______;
(2)DMP分子中C、H、O三种元素的质量比为____________;
(3)DMP分子中氧元素的质量分数为(结果精确到0.01)________。
低钠盐适合患有高血压、肾病、心脏病的患者服用,苹果酸钠盐(C4H8O5Na)是低钠盐的一种。请回答:
(1)苹果酸钠盐的相对分子质量是____________。
(2)苹果酸钠盐中各元素的质量比为C:H:O:Na= _________。
(3)若某病人每天食用5.85g苹果酸钠盐,比食用相同质量的食盐(Na Cl)少摄入钠元素多少克?(计算结果保留一位小数)
Cl)少摄入钠元素多少克?(计算结果保留一位小数)