氯化钠是一种重要的生活、生产必需品。下列叙述中正确的是( )
| A.锌粒与盐酸反应时,若加入适量氯化钠晶体,可加快反应速率 |
| B.标准状况下,氯化钠溶液呈中性,溶液的pH="7" |
| C.氯化钠中所含化学键为离子键,含离子键的化合物一定是离子化合物 |
| D.氯化钠溶液导电是化学变化,而熔融态氯化钠导电是物理变化 |
将标准状况下的aLHCl气体溶于1000g水中,得到的盐酸密度为密度为b g/cm3,则该盐酸的物质的量浓度是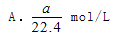
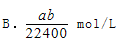
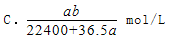

不另加试剂,用最简捷的方法来鉴别下列5种物质的溶液:①KOH;②Ba(NO3)2,③CuCl2,④NaCl,⑤MgSO4,则被鉴别出来的五种物质的先后顺序为
| A.①⑤②④③ | B.①③⑤④② | C.③①⑤②④ | D.⑤②①③④ |
一定量某营养液中溶质的配方分别如下:
配方一:0.3molKCl,0.2molK2SO4,0.1molZnSO4
配方二:0.1mol KCl,0.3mol K2SO4,0.1molZnCl2
配方一:0.3mol KCl,0.2mol K2SO4,0.1molZn SO4对于两种营养液的成分,下列说法中正确的是
| A.只有n(K+)相同 | B.只有n(Cl-)相同 |
| C.完全相同 | D.各离子的物质的量完全不同 |
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是
①过滤 ②加过量NaOH溶液 ③加适量盐酸④加过量 Na2CO3溶液 ⑤加过量 BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ | C.④②⑤①③ | D.⑤②④①③ |
欲配制100mL1.0mol/LNa2SO4溶液,正确的方法是
①将14.2g Na2SO4溶于100mL水中
②将32.2g Na2SO4•10H2O溶于少量水中,再用水稀释至100mL
③将20mL5.0mol/L Na2SO4溶液用水稀释至100mL.
| A.①② | B.①③ | C.②③ | D.①②③ |