物质结构理论有助于人们理解物质变化的本质,进行分子设计和研究反应规律。请回答下列问题:
(1)第三周期基态原子有2个未成对电子且电负性最大的元素是_____;
(2)金属晶体受到外力作用时易发生形变,而离子晶体容易破裂。试从结构的角度分析其中的主要原因____________;
(3)已知在水中存在平衡2H2O=H3O++OH-。下列分子中,中心原子采取的杂化方式与H3O+中氧原子的杂化方式相同的是_____
a.CH2=CH2中的碳原子 b.NH2-中的氮原子
c.ClO3-中的氯原子 d.NO2-中的氮原子
(4)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中Mg元素的质量分数为________。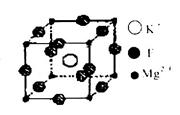
(1)在标准状况下4.48L CH4和CO2混合气体的质量为6.0g,则混合气体平均摩尔质量为 g/mol,相对于氢气的密度为 ;CH4和CO2的质量比为 .
(2)相同体积、相同物质的量浓度的AgNO3溶液,分别与相同体积的KCl、CuCl2、AlCl3溶液反应恰好完全反应,则KCl、CuCl2、AlCl3三种溶液的物质的量浓度之比为 。
(3)标准状况下,V L的某气体(摩尔质量为M g•mol﹣1)溶解在1L水(水的密度近似为1g•cm﹣3)中,假设气体完全溶解且不与水发生反应,溶液的密度为ρg•cm﹣3,则所得溶液的物质的量浓度c= mol/L.(选择以上字母表达计算式,要求化简).
现有0.540 kg质量分数为20%的CuCl2溶液。计算:
(1)溶液中CuCl2的物质的量;
(2)溶液中Cu2+和Cl-的物质的量。
在标准状况下,100mL某气体的质量为0.179g, 试计算这种气体的相对分子质量?
配制0.2mol/LNa2SO4溶液50mL,需要称取固体Na2SO4的质量是多少?
标准状况下CO与CO2的混合气体共22.4 L,其质量为36 g,求混合气体中CO与CO2的质量和体积各是多少?