下列实验装置中,实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是 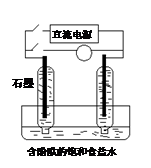
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl— Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,电子沿“b →Cu→电解质溶液→石墨→a”的路径流动 |
| C.断开K2,闭合K1时,铜电极附近溶液变红 |
| D.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl— |
下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:1的是()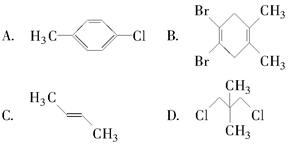
下列说法正确的是( )
A.棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O
B.蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N四种元素
C.用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO
D.向盛有少量苯酚稀溶液试管中滴加少量稀溴水,边滴边振荡,有白色沉淀出现
下列物质中含有亲水基团但不溶于水的是( )
| A.CH3CH2Br |
| B.CH3(CH2)11CH2OH |
| C.C17H35COONa |
D.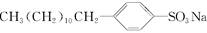 |
我国在反兴奋剂问题上的立场是坚决支持“人文奥运”的。某种兴奋剂的结构如下图所示。关于它的叙述正确的是()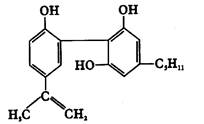
| A.它的分子式为C20H22O3 |
| B.它易溶于水 |
| C.它的分子中共平面的碳原子最多有16个 |
| D.1mol该物质发生化学反应时最多消耗7molH2和4mol Br2 |
将两种气态烃组成的混合气体0.1mol,完全燃烧后得到0.16mol二氧化碳和3.6克水, 则混合气体中()
| A.混合气体中一定有甲烷 | B.混合气体中一定有甲烷和乙烯 |
| C.混合气体中一定有乙烷 | D.混合气体中一定有乙炔 |