某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是
A.若溶液中c(A-)=c(Na+),则溶液一定呈中性
B.溶液中不可能存在:c(Na+)> c(A-)> c(OH-)> c(H+)
C.若c(OH-)> c(H+),溶液中不可能存在:c(Na+)> c(OH-)> c(A-)> c(H+)
D.若溶质为NaA、HA,则一定存在:c(A-)> c(Na+)> c(H+)> c(OH-)
已知 25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×10-5 |
4.9×10-10 |
Ka1=4.3×10-7 Ka2=5.6×10-11 |
则下列说法正确的是()
A.等物质的量浓度的各溶液 pH 关系为:pH ( NaCN)>pH(Na2CO3)>pH( CH3COONa)
B.浓度均为0.2mol/LNaHCO3和 Na2CO3溶液中,存在的粒子种类不相同
C.0.4 mol·L-1HCN 溶液与 0.2 mol·L-1NaOH 溶液等体积混合后,所得溶液中:c(Na+)>c(OH-)>c(H+)
D.25℃时,pH=4且浓度均为0.1 mol·L-1的 CH3COOH、CH3COONa混合溶液中:
c(Na+)+c(H+)>c(CH3COO-)+c(CH3COOH)
反应CH3OH ( l )+ NH3( g ) = CH3NH2( g ) + H2O ( g )在某温度自发向右进行,若反应|ΔH|= 17kJ. mol—1,|ΔH-TΔS|= 17kJ. mol—1,则下列正确的是()
| A.ΔH>0,ΔH-TΔS<0 | B.ΔH <0,ΔH-TΔS>0 |
| C.ΔH>0,ΔH-TΔS>0 | D.ΔH <0,ΔH-TΔS<0 |
工业制取硫酸是一个连续的生产过程。今测得进入接触室时混合气体(396 K、40000 kPa,主要成分为SO2、O2、N2)的流量为1.0 m3/s,从接触室导出气体(792 K、40000 kPa)的流量为1.8 m3 /s。据此,以下说法中正确的是( )
| A.SO2的催化氧化反应是吸热反应 |
| B.SO2的转化率一定为20% |
| C.导出气体中SO3所占的体积分数为2 / 9 |
| D.单位时间内进入接触室的气体与从接触室导出的气体的物质的量之比为9∶10 |
如图所示,甲容器容积不变,乙容器有可移动活塞。甲中充入3mol A和2 mol B,乙中充入2 mol C和2 mol D,发生反应:3A (g) + 2B(s)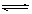 C(g) +D(g);△H>0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是()
C(g) +D(g);△H>0。在相同温度下反应达到平衡,活塞移动到4处。下列有关说法正确的是()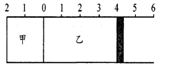
A.平衡后,容器内压强:p甲 >p乙
B.平衡后,若向乙中再加入B物质,活塞向右移动
C.同时升高相同温度,达到新平衡时,甲中A物质的速率等于乙中A物质的速率
D.平衡后,若将活塞移动至6处,乙中c(A),c(D)均减小
下列有关农业问题,所采取的措施或解释属于正确的是()
| A.铵态氮肥和草木灰(含K2CO3)能混合施用 |
| B.化肥和农家肥(如绿肥)不可混合施用 |
| C.“盐碱地”中有Na2CO3通过加石膏使之生成碳酸钙,这样根据平衡移动原理,随着c(CO32—)浓度的降低,“盐碱地”的碱性降低 |
| D.复合肥(如磷酸氢二铵)和生石灰能一起施用 |