短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是
| A.E是一种非金属元素 | B.在ECln中E与Cl之间形成共价键 |
| C.E的一种常见氧化物为EO | D.E位于元素周期表的ⅥA族 |
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应
SO2(g)+NO2 (g)  SO3(g)+NO(g)
SO3(g)+NO(g)
达到平衡,正反应速率随时间变化的示意图如下图所示。由图可得出的不正确结论是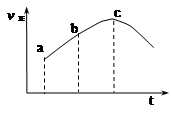
| A.反应物的总能量高于生成物的总能量 |
| B.反应物浓度:a点大于b点 |
| C.反应在c点达到平衡状态 |
| D.SO2的转化率:a点小于b点 |
CO(g)+H2O(g)  H2(g)+CO2(g)△H<0,在其他条件不变的情况下,下列说明正确的是
H2(g)+CO2(g)△H<0,在其他条件不变的情况下,下列说明正确的是
| A.加入催化剂,改变了反应的途径,反应放出的热量也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.若在原电池中进行,反应放出的热量不变 |
下列微粒中: ①13Al3+,② 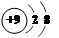 ,③
,③ 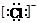 ,④F-,其核外电子数相同的是
,④F-,其核外电子数相同的是
| A.①②③ | B.②③④ | C.①②④ | D.①③④ |
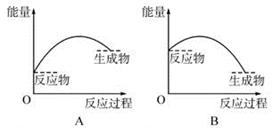
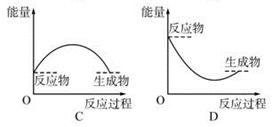
各图中,表示正反应是吸热反应的图是