下列相关离子方程式的书写正确的是( )
A.硫化亚铁溶于适量稀硝酸中: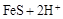 → → ↑ ↑ |
B.向水中通入少量氯气:Cl2 + H2O 2H+ + Cl﹣+ ClO﹣ 2H+ + Cl﹣+ ClO﹣ |
C.碳酸氢钠溶液中加入过量Ba(OH)2溶液: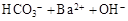 → →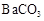 ↓ ↓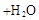 |
D.硫酸溶液中加入过量Ba(OH)2溶液: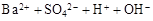 → →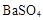 ↓ ↓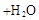 |
下列说法正确的是( )
| A.离子键就是使阴、阳离子结合成化合物的静电引力 |
| B.所有金属与所有非金属之间都能形成离子键 |
| C.在化合物CaCl2中,两个氯离子之间也存在离子键 |
| D.含有离子键的化合物一定是离子化合物 |
下列性质中,可以证明某化合物内一定存在离子键的是( )
| A.可溶于水 | B.具有较高的熔点 |
| C.水溶液能导电 | D.熔融状态能导电 |
下列各元素的原子在形成不同物质时,既能形成非极性键,也能形成极性键,还能形成离子键的是( )
| A.Na | B.Fe | C.C | D.Ne |
下列表示物质结构的化学用语或模型图正确的是( )
A.H2O2的电子式: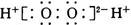 |
B.CS2的比例模型: |
C.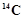 的原子结构示意图: 的原子结构示意图: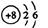 |
D.CCl4的结构式: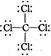 |
在下列变化过程中,被破坏的作用力正确的是( )
| A.干冰升华一一共价键 |
| B.二氧化硅熔融——范德华力 |
| C.氢氧化钠熔融——离子键、共价键 |
| D.硫酸氢钠溶于水——离子键、共价键 |