下列有关能量的判断或表示方法正确的是( )
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
B.从C(石墨) → C(金刚石)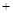 Q Q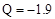 kJ,可知石墨比金刚石更稳定 kJ,可知石墨比金刚石更稳定 |
C.由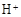 (aq) (aq) (aq) → H2O(l) (aq) → H2O(l)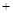 Q Q kJ,可知:含1mol CH3COOH的稀溶液与含1mol NaOH的稀溶液混合,放出热量等于57.3 kJ kJ,可知:含1mol CH3COOH的稀溶液与含1mol NaOH的稀溶液混合,放出热量等于57.3 kJ |
D.2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)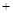 O2(g) → 2H2O(l) O2(g) → 2H2O(l)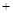 Q Q 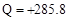 kJ kJ |
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图表示,在下列因素中,①盐酸的浓度,②镁条的表面积, ③溶液的温度,④氯离子的浓度,影响反应速率的因素是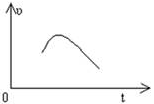
| A.①④ | B.③④ | C.②③ | D.①②③ |
下列说法正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大单位体积内活化分子的数目,有效碰撞次数增大,化学反应速率增大 |
| C.升高温度能使化学反应速率增大,唯一的原因是增加了反应物分子中活化分子的百分数 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
下列措施肯定能使化学平衡移动的是
| A.增大反应物的量 | B.增加压强 | C.升高温度 | D.使用催化剂 |
已知FeCl3和MnO2都可作H2O2分解制O2的催化剂,为了探究温度对化学反应速率的影响,下列实验方案可行的是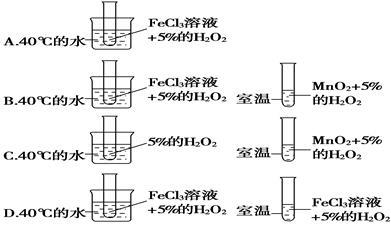
在测定中和热的实验中,下列说法正确的是
| A.使用环形玻璃棒是为了加快反应速率,减小实验误差 |
| B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 |
| C.用0.5mol·L-1NaOH溶液分别与0.5 mol·L-1的盐酸、醋酸溶液反应,如所取的溶液体积 相等,则测得的中和热数值相同 |
| D.在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计 |