下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将硫酸滴入装有亚硫酸钠固体的培养皿。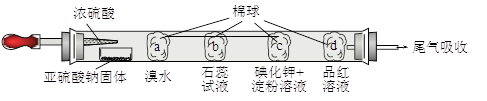
关于此实验的“现象”、“解释或结论”以及对应关系均正确的是
| 选项 |
现象 |
解释或结论 |
| A |
a处黄色褪去 |
非金属性:Br>S |
| B |
b处变为红色 |
二氧化硫与水反应生成酸性物质 |
| C |
c处变为蓝色 |
二氧化硫具有一定的氧化性 |
| D |
d处红色先褪去后恢复 |
二氧化硫具有漂白性且漂白性不稳定 |
下列四种溶液中,由水电离生成的氢离子浓度之比是( )
①pH=0的盐酸 ②0.1 mol/L的盐酸 ③0.01 mol/L的NaOH溶液 ④pH=14的NaOH溶液
| A.1∶10∶100∶1 | B.1∶10-1∶10-12∶10-14 |
| C.14∶13∶12∶14 | D.14∶13∶2∶1 |
现有常温时pH=1的某强酸溶液10 mL,下列操作能使溶液的pH变成2的是( )
| A.加水稀释成100 mL |
| B.加入10 mL的水进行稀释 |
| C.加入10 mL 0.01 mol/L的NaOH溶液 |
| D.加入10 mL 0.01 mol/L的HCl溶液 |
t℃时,水的离子积为KW,该温度下将a mol·L-1一元酸HA与b mol·L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是( )
A.混合液中,c(H+)=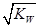 |
| B.混合液的pH=7 |
| C.a=b |
| D.混合液中,c(B+)=c(A-)+c(OH-) |
下列溶液肯定显酸性的是( )
| A.含H+的溶液 |
| B.能使酚酞显无色的溶液 |
| C.pH<7的溶液 |
| D.c(OH-)<c(H+)的溶液 |
25℃时,水的电离达到平衡:H2O H++OH- ΔH>0,下列叙述正确的是( )
H++OH- ΔH>0,下列叙述正确的是( )
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.降温,使平衡左移,c(H+)减小,溶液呈碱性 |
| D.将水加热,Kw增大,pH不变 |