煤的“气化”是使煤变成清洁能源的有效途径之一,其主要反应为:C+H2O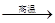 CO↑+H2↑。甲酸苯丙酯(F)是生产香料和药物的主要原料。下图是用煤为原料合成甲酸苯丙酯的路线图(部分反应条件和生成物已略去)其中D的分子式为C9H10O,且能发生银镜反应。
CO↑+H2↑。甲酸苯丙酯(F)是生产香料和药物的主要原料。下图是用煤为原料合成甲酸苯丙酯的路线图(部分反应条件和生成物已略去)其中D的分子式为C9H10O,且能发生银镜反应。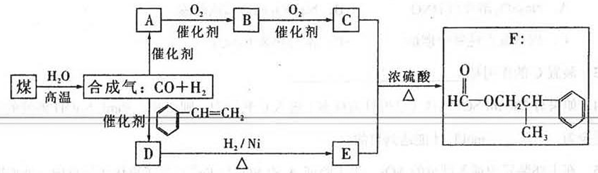
根据上述转化关系回答下列问题:
(1)写出A、D的结构简式:A:________________________ D:__________________________
(2)D→E的反应类型为_____________,B中的官能团是_____________。
(3)写山检验B中的官能团的试剂及出现的现象。
试剂_____________,现象_______________________________________。
(4)写出C与E反应生成F的化学方程式_______________________________________。
(5)“合成气”( CO、H2)除作合成有机物的原料外,还有其它用途,如_____________(举两例)。
(6)F有多种同分异构体,写出满足下列条件的两种同分异构体的结构简式。
①属于酯类,且能发生银镜反应。 ②苯环上的一氯取代物只有两种结构。
③分子结构中只有两个甲基。______________________________、______________________________
一定条件下,在一定体积的恒容密闭容器中,CO2与NH3在一定条件下反应生成尿素
CO2(g)+2NH3(g)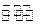 CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
根据题意完成下列各题;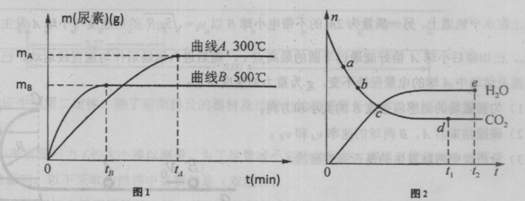
(1)500℃,用尿素表示该反应的反应速率,v(尿素)=mol/min.
(2)该反应的正反应△H0(填“>”或“<”)。
(3)上图2表示某温度时一些反应物与产物物质的量(n)随时间(t)变化的关系。
①对于该反应达到平衡状态的判断,下列说法正确的是。
| A.混合气体的密度不再发生改变 | B.图2中C点时,该反应达到了平衡状态 |
| C.混合气体的压强不再发生改变 | D.当消耗了2n mol NH3时,同时生成了n molH2O |
②反应速率v(CO2):图中点ab(填“>”、“<”或“=”)。
(4)用该原理生产尿素,工业上一般在220大气压下进行。其它条件不变,与常压相比,220大气压时NH3的转化率(填增大、减小或不变。)反应的平衡常数K(填增大、减小或不变)。
几种短周期元素的原子半径及某些化合价见下表:
| 元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
| 化合价 |
–1 |
–2 |
+4、–4 |
+4、–2 |
+5、–3 |
+3 |
+2 |
+1 |
| 原子半径/nm |
0.071 |
0.074 |
0.077 |
0.102 |
0.110 |
0.143 |
0.160 |
0.186 |
分析上表中有关数据,并结合已学过的知识,回答以下问题。涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中位于周期,族;
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
(3)A与J所形成化合物中的化学键类型是用电子式表示其形成过程
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
看右上图回答下列问题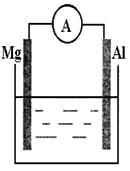
(1)若烧杯中溶液为稀硫酸,则观察到的现象是
,电流表指针(填偏转或不偏转),
两极反应式为:
正极;
负极。
(2)若烧杯中溶液为氢氧化钠溶液,
则负极为(填Mg或Al),总反应方程式为
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右下图所示:A、B两个电极均由多孔的碳块组成。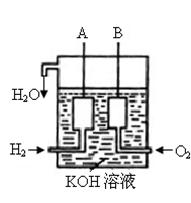
该电池的正极反应式为:。
(4)如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,电池的总反应方程式为:CH4+2O2+2KOH=K2CO3+3H2O,
则该电池的负极反应式为:。
用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
(1)实验过程如下图所示,分析判断________段化学反应速率最快,_______段收集的氢气最多。这段反应速率最快的原因是。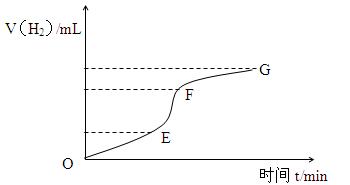
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是()
| A.蒸馏水 | B.氯化钠固体 |
| C.氯化钠溶液 | D.浓盐酸 |
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?
与氖原子核外电子数相同的四原子分子的化学式是,与氖原子核外电子数相同的五原子分子的结构式是,与氩原子核外电子数相同的四原子分子,既含极性键又含非极性键,它的电子式是,与氩原子核外电子数相同的单核离子,其原子核里含17个质子,20个中子,其化学符号是。