下列根据实验操作和现象所得出的结论可靠的是
| 选项 |
实验操作 |
实验现象 |
结 论 |
| A |
分别测定0.1mol/LNa2CO3和苯酚钠溶液的pH |
前者pH比后者的大 |
酸性:苯酚>碳酸 |
| B |
向无色溶液A中加入稀硫酸 |
产生淡黄色沉淀和无色气体 |
A中含S2O32-离子 |
| C |
CuSO4和H2SO4混合溶液中加入Zn |
锌表面附着红色物质;产生无色气体 |
氧化性:Cu2+>H+ |
| D |
向0.01mol/L的KCl、KI混合液中滴加AgNO3溶液 |
先出现黄色沉淀 |
溶解出Ag+的能力:AgCl > AgI |
市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹及人体排放的蛋白质油渍遇到它,皆能水解而除去。下列衣料中不能用加酶洗衣粉洗涤的是( )
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
| A.①②③ | B.②④ |
| C.③④⑤ | D.③⑤⑥ |
下列对于淀粉和纤维素的叙述中,正确的是
| A.互为同分异构体 | B.都是纯净物,化学性质完全相同 |
| C.碳、氢、氧元素的质量比完全相同 | D.结构相同 |
为验证淀粉水解可生成还原性糖,进行了如下实验:①取少量淀粉加水制成溶液;②加热煮沸;③加入新制的氢氧化铜悬浊液;④加入几滴稀硫酸;⑤再加热;⑥加入碱液中和并使溶液呈碱性。正确的操作排列顺序是
| A.①④⑤⑥③② | B.⑤④③②①⑥ | C.①④②⑥③⑤ | D.①⑤③④⑥② |
下列说法正确的是( )
| A.纤维素和淀粉遇碘水均显蓝色 |
| B.蛋白质、乙酸和葡萄糖均属电解质 |
| C.溴乙烷与NaOH乙醇溶液共热生成乙烯 |
| D.乙酸乙酯和食用植物油均可水解生成乙醇 |
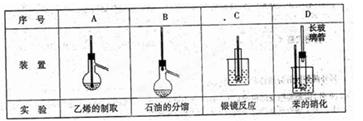
A-D是中学化学实验中使用温度计的装置示意图,其中所做的实验与装置不相符的是