水的电离平衡曲线如图所示。下列说法错误的是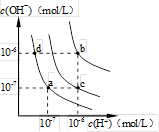
| A.水的电离常数KW数值大小关系为:b>c>d |
| B.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| C.温度不变,加入少量NaOH可使溶液从c点变到 a点 |
| D.在b点对应温度下,将pH=2的HCl与pH=10的NaOH溶液等体积混合后,溶液显中性 |
取某铁的氧化物样品,用140mL 5 mol/L盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下0.56 L氯气,使其中的Fe2+完全转化为 Fe3+,该样品中可能的化学式是( )
| A.Fe3O4 | B.Fe4O5 | C.Fe5O6 | D.Fe5O7 |
短周期元素X、Y、Z在元素周期表中的位置如右下图所示,下列说法正确的是( )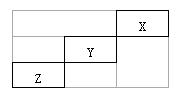
| A.X、Y、Z三种元素中,X的非金属性最强 |
| B.Y的原子半径比Z小 |
| C.Y的最高正化合价为+7 |
| D.Y的氢化物的稳定性比Z的氢化物弱 |
下列叙述不正确的是( )
A.向澄清石灰水中通入CO2产生白色沉淀 ,再通入过量CO2,沉淀消失 ,再通入过量CO2,沉淀消失 |
B.向AlCl3溶液中滴加NaOH溶液,产生白色沉淀,再加入过量NaOH溶液,沉淀消失 |
| C.向AgNO3溶液中滴加氨水,产生白色沉淀,再加入过量氨水,沉淀消失 |
| D.向Na2SiO3溶液中滴加盐酸,产生白色沉淀,再加入过量盐酸,沉淀消失 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.由2H2(g)+ O2(g)=2H2O(l) ΔH=" -571.6KJ·" mol-1可知,0.5 NA个H2分子完全燃烧生成气态水,放出的热量大于142.9 KJ |
| B.标准状况下,5.6 L SO2和5.6 L H2S混合后的气体分子总数为0.5 NA |
| C.Na2O2粉末与水反应,如产生0.5mol O2 ,则反应中转移电子数为NA |
| D.在1 L 0.1 mol/L醋酸钠溶液中, CH3COO- 离子总数为0.1 NA |
甲、乙、丙、丁分别是NaOH、Al2(SO4)3、MgSO4、BaCl2四种物质中的一种,若将丙溶液逐滴滴入甲溶液,发现开始时无沉淀,继续滴加产生沉淀,最终沉淀不消失,若将丙溶液滴入丁溶液产生沉淀,据此推断乙溶液是( )
| A.NaOH | B.Al2(SO4)3 | C.MgSO4 | D.BaCl2 |